2022 ASCO | PD-L1 IHC检测方法的选择影响胃癌免疫治疗的临床资格
导语:PD-L1状态在决定晚期胃癌患者是否使用ICIs中的作用因地而异。在美国,尽管临床指南推荐使用ICIs的强度是基于PD-L1表达的程度而异,但纳武利尤单抗和帕博利珠单抗的使用指征并不依赖于PD-L1状态,而当肿瘤CPS≥5时指南强烈推荐使用免疫检查点抑制剂(ICIs)。而在欧洲,纳武利尤单抗的使用仅限定在PD-L1 CPS≥5的患者。鉴于PD-L1 CPS在治疗选择中的核心作用,准确的评估至关重要。
根据新加坡国立大学Ryan Yong Kiat Tay在2022年ASCO年会上发表的一项研究(摘要:4026),用于胃癌患者PD-L1阳性检测的不同免疫组化(IHC)方法可产生显著不一致的结果。在胃癌指征需要PD-L1阳性才可使用ICIs的地区,这种差异可能会影响使用ICIs的资格。
研究摘要
PD-L1 IHC方法的选择影响胃癌免疫治疗的临床资格
Abstract 4026: Choice of PD-L1 immunohistochemistry assay influences clinical eligibility for gastric cancer immunotherapy
第一作者:Ryan Yong Kiat Tay
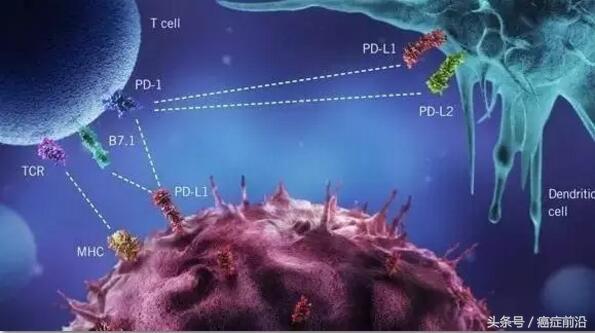
背景:免疫检查点抑制剂(ICIs)是目前转移性胃癌的标准治疗方法。为指导进行ICIs治疗的患者选择,程序性死亡配体-1(PD-L1)生物标志物表达常规通过免疫组化(IHC)来进行评估。监管机构批准ICI是基于PD-L1表达状态、使用综合阳性评分(CPS)等指标所进行的评分。然而,随着越来越多的ICIs获批,在各自的里程碑试验中,不同ICIs都匹配了不同的PD-L1抗体IHC检测方法,不同PD-L1 IHC检测方法是否可以统一目前尚不清楚。因此,新加坡国立大学永卢林医学院的Ryan Yong Kiat Tay等研究了胃癌PD-L1 IHC中所用的Dako 22C3、Dako 28-8 、Ventana SP-142检测试剂是否可以互换。
方法:该研究为横断面研究,样本在新加坡国立大学医院通过活检或切除胃癌获得。使用多重免疫组织化学/免疫荧光技术对362份胃癌样本的PD-L1 CPS、肿瘤细胞阳性比例评分(TPS)和免疫细胞(IC)进行评分。344个样品被制作成组织微阵列(TMA), 18个样本作为整片进行正交验证(orthogonal validation)。全片分析的样本来自接受ICI治疗的GC患者。
结果:使用28-8测定法检测,在临床相关CPS≥1、≥5和≥10时PD-L1阳性样本的百分比(表1)约是使用22C3测定法的2倍(CPS≥1:70.3% vs. 49.4%,P<0.001;CPS≥5:29.1% vs. 13.4%, P<0.001;CPS≥10:13.7% vs. 7.0%,P=0.004)。根据28-8测定法评估的平均CPS评分几乎是22C3测定法的2倍(6.39±14.5 vs. 3.46±8.98, P<0.001)。在临床重要的CPS≥5界值上,22C3测定法和28-8个测定法也仅中度一致。
表1. 临床相关CPS ≥1、≥5和≥10时,PD-L1阳性样本比例

结果:本研究结果表明,与使用22C3和其他测定法相比,使用28-8测定法对PD-L1进行评分,可能会导致更高的PD-L1阳性比例和更高的PD-L1评分。在临床上,这可能会导致更多的患者符合条件并被批准进行ICIs治疗。如果检测方法可以互换,那么根据所选择的检测方法,大量患者可能被不准确地拒绝或给予ICIs治疗。因此,在发现分析方法间具有一致性的更有力证据之前,我们强烈建议在将分析方法同等对待时需要谨慎。
研究者说

Dr. Raghav Sundar
主要作者、新加坡国立大学癌症研究所的Raghav Sundar评论指出,PD-L1 IHC 28-8测定法产生阳性结果的可能性大约是PD-L1 IHC 22C3测定法的2倍。而在纳武利尤单抗加化疗的关键性CheckMate-649试验中使用的是PD-L1 IHC 28-8测定法,在帕博利珠单抗+曲妥珠单抗+化疗治疗胃癌的关键性KEYNOTE-811试验中使用的是PD-L1 IHC 22C3测定法。28-8、22C3这两种PD-L1 IHC检测方法的差异对于患者具有实际意义,因为PD-L1表达的程度会影响检查点抑制剂的使用或推荐使用。
本质上,本研究强调这两种检测抗体是不可互换的。这两种PD-L1抗体似乎与PD-L1蛋白的不同部分结合,导致不同的细胞显示为阳性。展望未来,Sundar建议,使用22C3抗体重新评估CheckMate-649试验的结果可能会有好处。而对于临床医生来说,如果不同的结果会影响治疗的选择,可以考虑同时进行两种染色。
专家点评

Dr. Shaalan Beg
UT西南分校Harold C. Simmons综合癌症中心的Shaalan Beg对该研究进行了点评。
临床医生、临床研究者甚至患者都对PD-L1表达的定义感到困惑。PD-L1表达是对免疫治疗和免疫检查点抑制剂反应的生物标志物之一。但该领域的挑战在于,有多种检测方法定义了PD-L1表达的各种标准。在不同的临床试验中,PD-L1表达阳性的定义也有所不同。
而对于PD-L1抗体的IHC检测方法,我们有Dako 22C3、Dako 28-8以及Ventana SP-142。不同的临床试验在不同的PD-L1表达水平使用了不同的检测方法。因此,不同的地方、不同医生和不同实践小组使用不同的分析,就可能会有不同的解释。
本试验告诉我们,如果使用Dako 28-8就会识别出更高比例的PD-L1阳性患者,无论使用的界值是1%、5%还是10%(表1)。这就引发了一个问题,即这些分析在日常实践中如何使用。如果使用28-8检测,那么我们会发现更多PD-L1阳性的患者,而如果使用另一种检测,我们可能会漏掉PD-L1阳性的患者。
因此,我们需要协调怎样定义PD-L1的表达。我们需要更多分析不同检测方法一致性的数据,这样我们才能为正确的患者找到正确的药物和正确的生物标志物。这是当今困扰临床实践的一个问题。我们呼吁更好的前瞻性数据、并呼吁在不同测定方法和不同试验之间具有一个共识。

















评论