新型高强度、极低本体荧光的碳化光子晶体结构色编码液相芯片取得新进展



郑州大学第一附属医院杨建军教授、东南大学谢卓颖教授和北京航空航天大学郑付印副教授合作,构建了一种新型高强度、极低本体荧光的碳化光子晶体结构色编码的液相芯片体系,拓展了基于流动编码微载体的高通量、高灵敏、快速生物多元分析的新方法。
此新型多功能编码微载体具备良好的生物相容性,结构稳定性,功能修饰性和多元编码特性,将在细胞捕获和培养,多功能微载体,多器官悬浮芯片等生物多元编码和分析中取得广泛应用。相关成果发表在Research上。
研究背景
东南大学顾忠泽教授很早提出并实现了球形光子晶体编码液相生物芯片的构想,此光子晶体微载体编码作为国际上一种新型的代表性的光谱编码方式获日内瓦国际发明博览会特别金奖,已广泛应用于高通量、高灵敏、快速生物多元分析,尤其是在生物医学领域。
传统的光子晶体微球一直是由基于布拉格衍射原理产生的反射谱编码,编码的信息仅位于微球球形的顶点,根据目前的光谱测量技术,当微球足够小时,光谱采集非常困难。
同时,由于其本体荧光依然会导致很强的背景干扰,会在基于荧光读取的检测应用中对检测敏感度或可靠性产生负面影响。
由于组装粒子之间弱的粘附性,那些作为细胞捕获和培养载体的微球很容易被生长在表面的细胞破坏或内吞,导致细胞损伤和载体破坏。
因此,急需开发一系列形貌和构建材料组合可控的更具有理想特性和明显优势的新型光子晶体编码微球,并解决此液相芯片研究中流动编码载体的编码方法、功能特性、检测技术和规模制造等瓶颈问题。
研究进展
郑州大学第一附属医院杨建军教授、东南大学谢卓颖教授和北京航空航天大学郑付印副教授合作,构建了一种新型高强度、极低本体荧光的碳化光子晶体结构色编码的液相芯片体系,拓展了基于流动编码微载体的高通量、高灵敏、快速生物多元分析的新方法。
前期研究已证实聚多巴胺的黏附性、黑色素性质及基团活性可以赋予光子晶体高的机械强度、颜色可见度及灵活的生物分子的修饰( ACS Applied Materials & Interfaces, 2018, 10: 29378-29384;Nanoscale, 2018, 10: 3673-3679;ACS Applied Nano Materials, 2019, 2: 5752-5760. )。
作者也进行了传统光子晶体编码微球在多元细胞捕获、三维培养、缓释载体和结构色传感等方面的研究( Advanced Materials, 2014, 26(43): 7333-7338,Small, 2014, 10, 1, 88-93,ACS Applied Materials & Interfaces, 2016, 8 (22), pp 13840–13848)。
本文中,作者通过液滴限域的微流体技术组装单分散聚多巴胺包裹的二氧化硅纳米颗粒(PDA@SiO2),然后热分解得到碳化的光子晶体结构色编码微球(C@SiO2 PC beads),借助聚多巴胺的黏附性实现了更稳定的机械强度和结构色编码,且碳化后进一步赋予了极低的本体荧光。
此新型多功能编码微载体具备良好的生物相容性、结构稳定性、功能修饰性和多元编码特性,将在细胞捕获和培养、多功能微载体、多器官悬浮芯片等生物多元编码和分析中取得广泛应用。
在碱性条件下聚合多巴胺可均匀地涂附在二氧化硅粒子表面形成聚多巴胺壳,得到核壳结构PDA@SiO2粒子。
然后,利用基于微滴的微流体技术,将该粒子组装成球型PDA@SiO2微球。
最后,在无氧条件下对微球进行热解处理,得到高强度结构色C@SiO2微球。
利用上述微流控技术,PDA@SiO2粒子基于表面PDA的黏附性可以直接组装成稳定的PC结构的球型,与传统工艺相比,省去繁琐的高温灼烧处理。
PDA作为良好的碳源,经过碳化后可形成类石墨结构的碳,从而使微球在颜色和机械强度方面得到稳定提升(图1)。
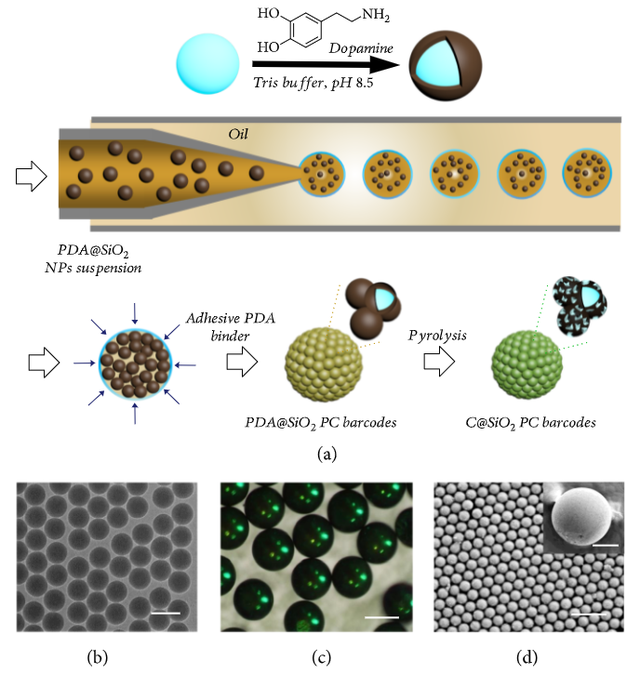
图1 C@SiO2结构色微球的纳米粒子制备、限域组装流程示意图和微纳结构表征
根据光子晶体的光学原理,用布拉格衍射方程可计算C@SiO2 PC微球的中心衍射波长(结构色),即λ= 1.633×d×na,其中λ是中心衍射波长,d是两个纳米粒子之间的中心到中心的距离,na是C@SiO2珠的平均折射率。因此调节组装粒子的尺寸即可调节微球的颜色。
通过调节粒子粒径制备的四种不同颜色的C@SiO2结构色微球,从图片可观察到这四种微球都具有明显可辨识的颜色,通过分析颜色编码与光谱编码信号采集面积的比较,可得出颜色编码比光谱编码在信号采集方面有极大的优势。(如图2所示)
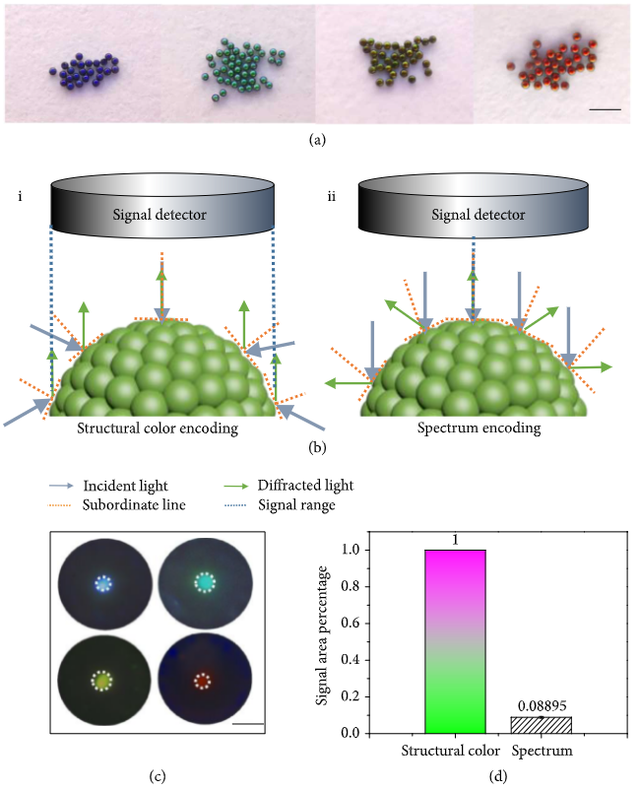
图2 通过调节粒子粒径制备的四种不同颜色的C@SiO2结构色微球,以及结构色编码的原理示意图和光学特性
根据C@SiO2微球、PDA@SiO2微球和SiO2微球在不同波段刺激下的荧光照片可得出,C@SiO2结构色微球具有更低的本体荧光(图3)。
此外,通过抗压及抗超声损伤实验也验证了C@SiO2结构色微球比PDA@SiO2微球及SiO2微球具有更高的机械强度。
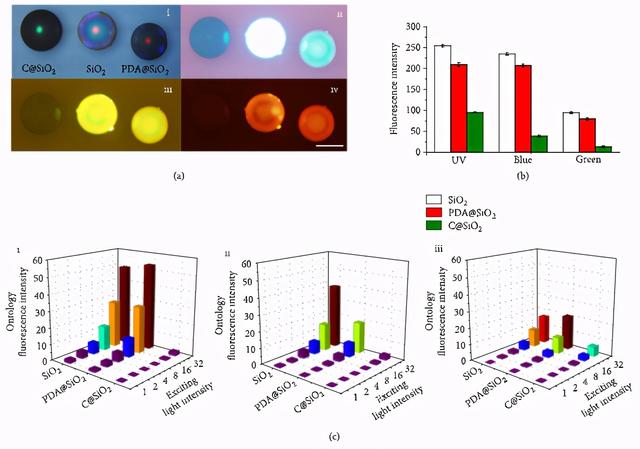
图3 光子晶体编码微球的超低本体荧光特性
基于结构色的多元编码特性,不同结构色的微球表面可以修饰不同的靶向功能探针,实现对多重细胞的同时捕获、培养、分离和多元分析。
作者在定性和定量表征编码微球具有良好生物相容性后,将C@SiO2微球经多聚赖氨酸修饰后进行细胞的捕获和共培养,发现细胞可被捕获并贴壁生长在微球表面进行三维悬浮培养,经共培养7天后,细胞增殖密度非常大并完全覆盖微球表面,在这个过程中微球依然可以保持原有的球体形状及结构色。
将C@SiO2微球捕获的细胞进行相应的细胞核(Hoechst 33342)和细胞膜(DiO)的荧光染色,蓝色的细胞核荧光和绿色的细胞膜荧光信号均可以很容易辨识,消弱了细胞信息分析期间微载体背景荧光的干扰,简化了细胞荧光信号的提取。
所有这些结果表明,C@SiO2微球不仅能在细胞捕获和培养过程中保持良好的机械稳定性和颜色可见性,而且用荧光标记细胞后具有良好的荧光读取能力(图4)。
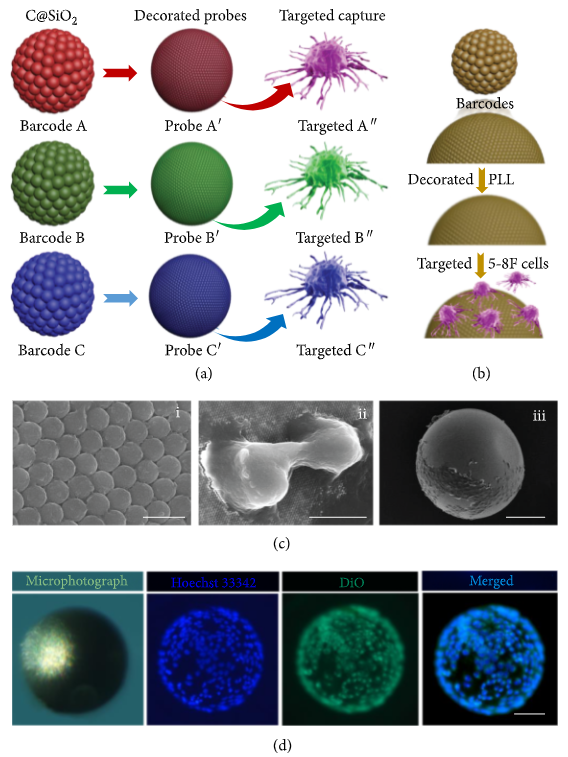
图4 新型光子晶体编码微球在细胞捕获,培养及多元分析检测的应用
未来展望
光子晶体具有独特的光学和结构特性,球形自组装光子晶体的特征反射峰具有检测角度无关性及分级耦合和协同放大效应,基于此液相悬浮编码微载体的多元分析由于其高灵活性、快速检测及良好的重复性在多元定量检测,尤其是生物医学领域具有广泛的应用。
以此多元编码微载体体系为基础,未来将通过发展限域可控组装等技术手段开发一系列形貌和构建材料组合可控的新型光子晶体微载体,解决、优化和发展流动编码载体的编码方法、检测技术等瓶颈问题,以及打破规模制备工艺的局限性,努力实现从实验室样本转换为实际产品,服务于医院及研究机构用于肿瘤等临床疾病的诊断和分析。
这项工作得到了中国博士后科学基金、国家自然科学基金、北京市科技新星计划、北航青年拔尖创新人才支持计划等项目的资助。特别感谢东南大学生物电子学国家重点实验室在工作中给予的支持和帮助。
作者简介
- 杨建军
主任医师,教授,郑州大学第一附属医院麻醉与围术期医学部主任,郑州大学医学科学研究院神经科学研究所副所长,担任中国精准医学学会常务理事、中华医学会麻醉学分会常务委员;国家自然科学基金、法国国家科研署(ANR)及荷兰科学研究会(NWO)等基金评审专家。
主要研究方向:1)全麻机理及术后认知功能障碍;2)疼痛、抑郁、认知损伤共病的机制研究;3)大数据及人工智能;4)微纳材料与医学的交叉学科研究。
- 谢卓颖
东南大学青年首席教授,生物电子学国家重点实验室主任助理、生物医学工程国家教学示范中心副主任。
主要从事微纳功能材料、生物传感与生物成像、器官芯片等研究。
主持国家自然基金、江苏省自然科学基金、国家重点研发计划子课题等多项国家与省部级科研项目。已在国内外知名期刊上发表论文60余篇,申请中国发明专利30余项,获授权20余项。
- 郑付印
北京航空航天大学生物与医学工程学院和北京市生物医学工程高精尖创新中心双聘副教授,博士生导师,北京市科技新星计划,江苏省“优博”,北航“青拔”。
曾依次为东南大学和中国航天员中心联培博士,美国加州大学伯克利分校访问学者,麻省理工学院博士后和新加坡南洋理工大学Research Fellow。
重点围绕在地基和面向空间应用的人体类器官和器官芯片,3D和4D生物打印,仿生结构色功能材料和航天医学工程等领域进行深入的研究,并建立了仿生类器官和器官芯片实验室(Bioinspired Organoids & Organ-on-a-Chip,BOOC Lab)。
主持和参与9项国家自然科学基金项目(重点2项,面上1项,青年2项),在PNAS,Adv. Mater.,Research等发表30余篇学术论文,已授权10项发明专利。
担任中国创新型医院学会医工转化与健康产业融合专业委员会委员,中国微循环学会转化医学分会委员会委员。
来源:微信公众号“Research科学研究”



















评论