BRCA突变卵巢癌患者一线维持治疗结果喜人
编译:肿瘤资讯编辑部
来源:肿瘤资讯
2018年 11 月 23 日-25 日,欧洲肿瘤内科学会亚洲年会 (ESMO Asia 2018) 在新加坡盛大召开。本次大会上,多项重磅研究报道,其中,来自澳大利亚威尔士亲王医院的Michael Friedlander教授口头报道了SOLO1研究主要结果: BRCA1/2突变(BRCAm)的初治晚期卵巢癌一线含铂化疗后给予奥拉帕利维持治疗,这一研究作为本次的LBA重磅发布。大会现场,Andres Maria Poveda Velasco教授对SOLO1研究进行现场点评。

LBA3 BRCA1/2突变(BRCAm)的初治晚期卵巢癌一线含铂化疗后给予奥拉帕利维持治疗:III期SOLO1研究

图:Michael Friedlander教授大会现场报告
背景
约25%的卵巢癌患者为高级别浆液性治疗,携带致死性BRCA突变,其中胚系突变后体细胞突变的患者比例分别占75%和25%。40%BRCA突变相关的卵巢癌患者没有卵巢癌或乳腺癌家族史。BRCA突变型和非BRCA突变型卵巢癌的管理相似,手术后给予铂类为基础的化疗,后定期观察随访,然而大多数的患者会在诊断后2-3年复发。在卵巢癌患者中,合并致死性BRCA突变是一个相对预后好的因素。BRCA突变的卵巢癌患者接受铂类为基础的化疗,可以取得较高的缓解率,达到88%;此外,BRCA突变型卵巢癌接受化疗的PFS相比于非BRCA突变的卵巢癌患者更长。
总体而言,FIGO III-IV期的BRCA突变型卵巢癌患者的10年生存率为20-30%。新诊断的晚期卵巢癌患者是唯一有可能治愈的患者。铂类治疗敏感的复发性卵巢癌患者,接受PARP抑制剂维持治疗后,可以显著延长PFS。在SOLO2研究中,奥拉帕利对比安慰剂维持治疗的PFS分别为19.1 vs 5.5个月,HR 0.30(95%CI:0.22-0.41),P<0.0001。目前,奥拉帕利已经在美国、欧盟、日本、中国等多个国家地区获批用于铂类敏感复发的卵巢癌,无论患者的BRCA突变状态。随机、双盲、全球SOLO1研究是第一项III期研究,在接受了一线含铂化疗后的BRCA突变型初治晚期卵巢癌患者中评估奥拉帕利维持治疗。
方法
SOLO1研究入组了新诊断的III-IV期,高级别浆液性或子宫内膜型卵巢癌,原发腹膜癌或输卵管癌,合并胚系或体细胞BRCA突变,ECOG PS 0-1分,接受了减瘤手术,铂类为基础化疗后,取得临床完全或部分缓解。患者随机2:1分配接受奥拉帕利300 mg,bid(N=260)或安慰剂(N=131)治疗。患者接受维持治疗直至疾病进展;在完成2年治疗后疾病未进展的患者停药;在完成2年治疗时取得PR的患者可以继续接受维持治疗。主要终点为研究者评估的无进展生存期(PFS;改良RECIST v1.1标准评估)。
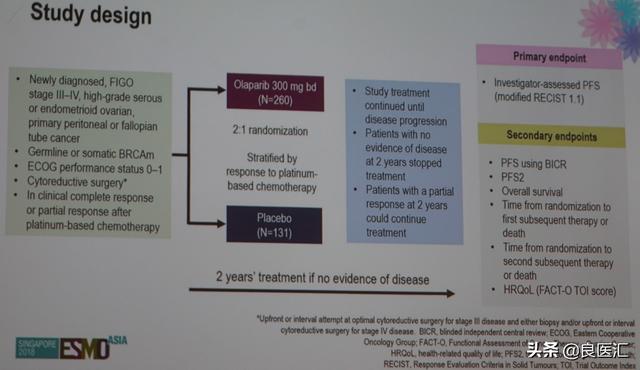
图:SOLO1研究设计
结果
参与随机的391例患者,260例接受奥拉帕利治疗,130例接受安慰剂治疗(1例随机患者未接受安慰剂治疗)。两组患者的基线特征均衡。一线化疗后取得临床完全缓解的患者,奥拉帕利组和安慰剂组分别达到81.9%和81.7%。患者的中位随访时间为41个月。对比两组患者的维持治疗情况,未完成2年治疗的患者,奥拉帕利组和安慰剂组分别为42.7%和70.8%;按照方案完成2年治疗的患者分别占47.3%和26.9%。在未完成2年治疗前,因为疾病进展导致停药的患者,奥拉帕利组和安慰剂组分别为51例(19.6%)和78例(60.0%);两组的中位治疗持续时间分别为24.6和13.9个月。
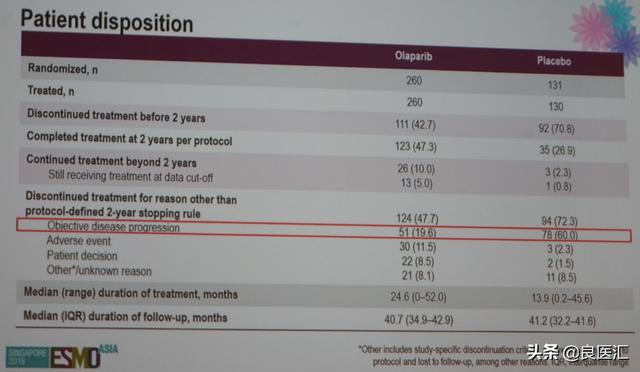
图:两组患者的维持治疗情况
主要终点PFS分析显示,奥拉帕利维持治疗对比安慰剂,可以显著延长PFS,降低70%的疾病进展或死亡风险,两组的mPFS分别为尚未达到和13.8个月,HR 0.30;95%CI:0.23-0.41;P<0.0001。进一步根据K-M分析,3年时仍未出现疾病进展或死亡的患者,奥拉帕利组和安慰剂组分别为60.4%和26.9%。PFS亚组分析显示,各个亚组均观察到一致的PFS获益。
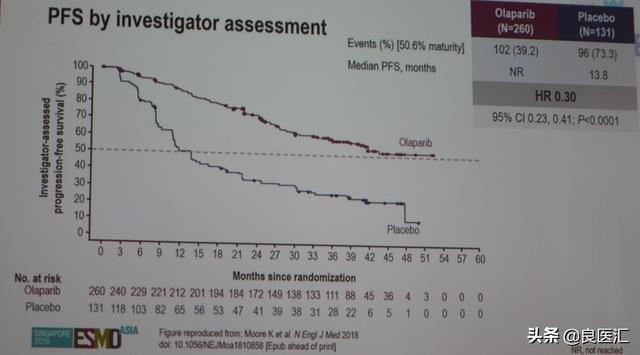
图:两组的PFS对比
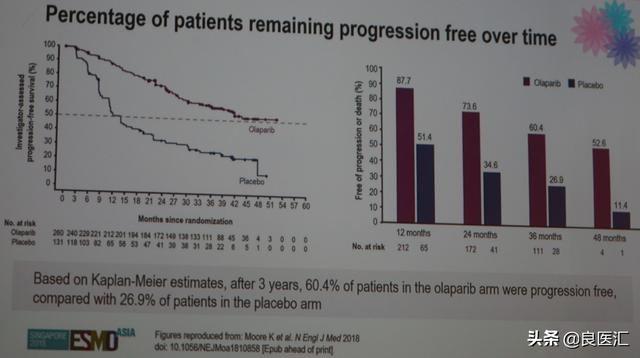
图:未达到PFS终点的患者比例
研究者进一步进行了PFS2分析,即随机至第二次治疗进展或死亡的时间,在研究药物进展后,安慰剂组和奥拉帕利组分别有35%(33/94)和11%(10/91)的患者接受了PARP抑制剂治疗。PFS2分析显示出与主要终点PFS一致的结果,两组的mPFS2分别为尚未达到和41.9个月,HR 0.50(95%CI:0.35-0.72),P=0.0002。
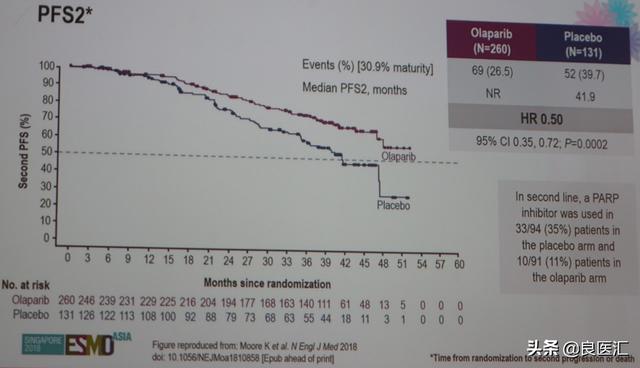
图:两组的PFS2对比
研究者进一步分析了其他疗效终点指标,如至第一次后续治疗或死亡的时间,至第一次后续治疗或死亡的时间等,均观察到奥拉帕利组一致的获益,见下图。
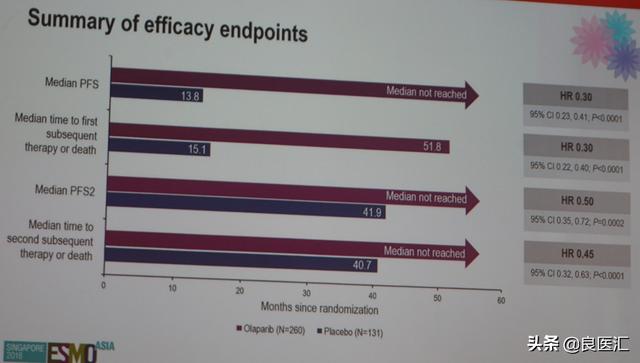
图:疗效终点指标总结
生活质量对比:研究者同时对比了奥拉帕利组和安慰剂组的生活质量,结果显示,两组自基线开始至24个月的FACT-O TOI评分差异无显著临床意义。
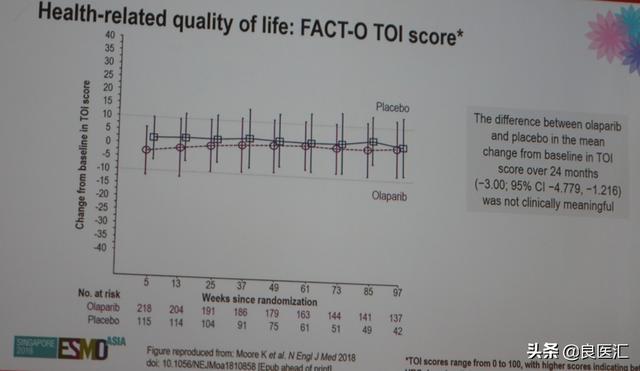
图:两组的生活质量对比
大多数的不良事件(AE)为低级别,最常见的≥3级毒性,奥拉帕利组为贫血(22%)和中性粒细胞减少(8%)。奥拉帕利剂量减低、中断、停药的发生率分别为28%、 52%和12%。值得关注的AE,如MDS/AML发生率,奥拉帕利组和安慰剂组分别为1.2%和0;新发的第二原发肿瘤,两组发生率分别为1.9%和2.3%;肺炎/ILD发生率,两组分别为1.9%和0。
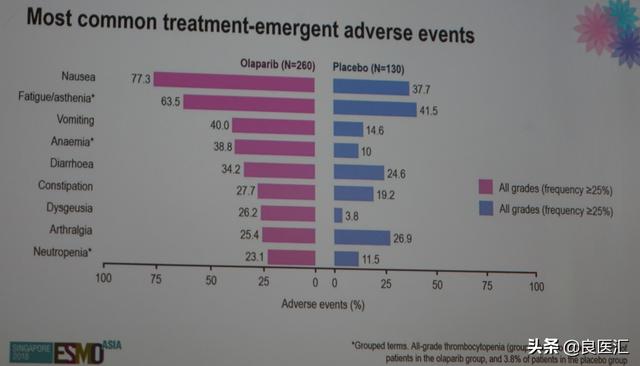
图:两组的安全性对比
结论
奥拉帕利对比安慰剂维持治疗用于一线含铂双药化疗后取得客观缓解的初治BRCA突变型卵巢癌患者,可以显著延长近3年的mPFS。奥拉帕利维持治疗组的生存曲线在2年后无明显变化,提示即使停止治疗,仍观察到明显的持续治疗效果。此外,奥拉帕利组的PFS2也显著更优,提示奥拉帕利维持治疗并不会影响患者从后续治疗中获益。总体而言,奥拉帕利治疗的耐受性好,安全性与其用于复发性患者的治疗一致。基于这一研究结果,奥拉帕利应该被推荐作为BRCA突变型初治疗卵巢癌患者,在接受铂类为基础化疗后取得客观缓解患者的维持治疗方案。建议所有卵巢癌患者在诊断时就应该检测BRCA突变状态。
Andres Maria Poveda Velasco教授大会现场点评

图:Andres Maria Poveda Velasco教授大会现场点评
BRCA突变型卵巢癌约占所有卵巢癌患者的20-25%,这类患者对铂类为基础的化疗敏感,缓解率较高,达到88%;且相比于非BRCA突变型卵巢癌,可以取得显著更长的PFS。关于BRCA突变型卵巢癌患者的预后是否优于非BRCA突变型,目前尚未明确。目前,已有3个PARP抑制剂维持治疗获批用于复发性高级别卵巢癌患者,奥拉帕利、niraparib和rucaparib,在所有铂敏感复发的卵巢癌患者中均观察到PARP抑制剂维持治疗的疗效,但是BRCA突变型肿瘤的预后更高。在上述PARP抑制剂维持治疗的研究中,均未观察到患者OS的获益,但在Study 19研究中,有10%的长期获益者,接受PARP抑制剂治疗6年以上尚未出现肿瘤进展。目前,PRAP抑制剂的耐药仍然是当下的临床难题,即使是BRCA突变的患者,治疗后也会出现耐药。
BRCA突变型患者相比于BRCA野生型患者是否有更好的预后呢?在GOG218研究中,即紫杉醇卡铂对比紫杉醇卡铂联合贝伐珠单抗再行贝伐珠单抗维持治疗的研究中,两个治疗组患者的PFS无显著差异;似乎BRCA1/2突变患者的PFS优于野生型患者。SOLO1研究入组了初治晚期卵巢癌患者,大多数的患者接受了减瘤手术,两组分别为61.9% vs 64.9%,患者接受奥拉帕利维持治疗2年或直至疾病进展,对比两组患者的3年无进展率,发现奥拉帕利组显著高于安慰剂组,分别为60.4%和26.9%。SOLO1研究取得了非常喜人的阳性结果,目前奥拉帕利组的mPFS尚未达到,60.4%的患者3年时未出现进展,在中位至第一次后续治疗对比上,奥拉帕利对比安慰剂,显著延长后线治疗的时间,两组的绝对差值为36.7个月。目前,OS数据尚未成熟,PFS2可以作为OS的替代指标。安慰剂组,35%的患者在第一次进展后接受了PARP抑制剂治疗;在随机后48个月,奥拉帕利组有60%的患者未出现第二次进展。中位至第二次进展时间,奥拉帕利组尚未达到,但两组对比,奥拉帕利组显著更优,HR 0.5;P=0.0002。
基于SOLO1研究结果,可以给我们哪些启示呢?PARP抑制剂目前已经在无论BRCA突变状态的铂类敏感复发性卵巢癌患者中取得广泛适应症。指南推荐,对于所有卵巢癌患者都建议进行胚系BRCA突变检测,可以判断预后,预测患者治疗疗效,并发现BRCA突变携带者。SOLO1研究的结果进一步强调了早期进行BRCA检测的重要性。那么,目前的问题是,BRCA突变的患者应该是一线使用还是复发后使用PARP抑制剂?
作为第一项随机III期临床研究,SOLO1有如下几个优势:第一,这是一项设计非常严谨的研究,入组了BRCA突变的患者;第二,统计学设计良好,对照组的mPFS达到13.8个月,达到了既定的mPFS统计假设;第三,BRCA突变是一个非常好的标志物,是真正的靶向治疗,这一研究也是精准治疗的体现;第四,研究取得了有意义的临床获益,观察到患者显著的PFS获益,很高比例的患者在3年时仍未出现疾病进展;第五,两组的毒性无显著差异,生活质量也无临床有意义的差异;第六,在完成24个月的既定药物治疗后,仍观察到持续的获益,90%的患者在治疗2年时停药,但3年PFS率高达60%。
最后,关于SOLO-1研究,仍有一些问题值得讨论。首先,在gBRCA突变型患者中的研究结果是否可以拓展至sBRCA突变患者?第二,对照组是否是全球接受的标准治疗方案,在很多地区,贝伐珠单抗维持被推荐作为标准治疗。第三,PARP抑制剂维持治疗是否应该被前移至一线?我们是否可以建立一个新的PARP抑制剂维持治疗模式,如BRCA突变患者一线PARP抑制剂维持,BRCA野生型患者,复发后PARP抑制剂维持,需要等待PAOLA和PRIMA研究结果。第四,2年的PARP抑制剂治疗是否足够?90%的患者在2年时停药,但3年无进展PFS率高达60%;贝伐珠单抗和其他药物的维持治疗经验是否可以借鉴?在study 19研究中观察到后期获益。第五,PARP抑制剂治疗进展后,再次接受PARP抑制剂治疗是否同样获益?二线治疗时,安慰剂组和奥拉帕利组分别有35%和11%的患者接受PARP抑制剂治疗,这一问题有待OREO研究解答。
版权声明
版权属肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。




















评论