新加坡开展“先信使、后科兴”计划,收集更多的疫苗安全数据
为了解不同冠病疫苗的免疫保护作用,卫生部将与国家传染病中心合作,邀请3600名对首剂信使核糖核酸(mRNA)冠病疫苗过敏的人接种两剂科兴疫苗,并监测是否出现副作用。
“先信使、后科兴”
卫生部将与国家传染病中心合作,开展“先信使、后科兴”计划(Sinovac After mRNA,简称SAM),监测部分参与研究的接种者是否出现副作用。
科兴疫苗尚未被纳入新加坡的全国疫苗接种计划,目前只有采用mRNA技术的辉瑞/复必泰(Comirnaty)和莫德纳疫苗属于全国计划。
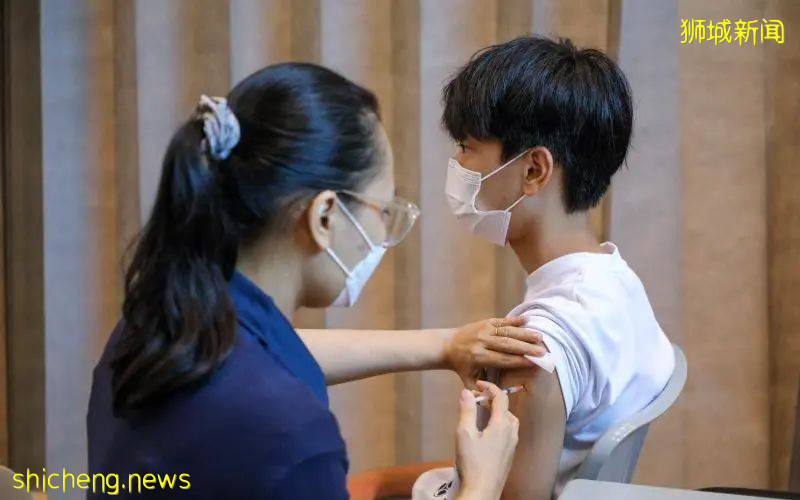
受邀加入“先信使、后科兴”的人,得到公共医院的诊所接种,以便当局密切监测是否出现副作用,以及收集更多疫苗安全数据。
接种者必须在接种科兴疫苗后的第一、第三和第七天接受问卷调查,通报是否出现任何症状或反应。
领导这项研究的是国家传染病中心高度隔离病房主任林宝莲副教授,她也是卫生部冠病疫苗专家团成员。
卫生部已联系约3600名对首剂mRNA冠病疫苗过敏者,超过1400人表示有兴趣。卫生部将通知他们如何参加并免费接种科兴疫苗。
“新加坡冠病疫苗免疫反应和保护作用”
国家传染病中心也将邀请SAM计划的其中200名受试者,参与另一项名为“新加坡冠病疫苗免疫反应和保护作用”(Singapore COVID-19 Vaccine Immune Response and Protection Study,简称SCOPE)的研究。
这项由国家传染病中心顾问医生巴纳比·扬(Barnaby Young)领导的大型研究,旨在了解对首剂mRNA冠病疫苗过敏者,接种科兴疫苗后的免疫反应和免疫期。
受试者须在接种每剂科兴疫苗后,以及接种后的两个月、六个月和12个月进行抽血检测。
诺瓦瓦克斯重组蛋白疫苗
卫生部长王乙康上周透露,新加坡已经同美国医药公司诺瓦瓦克斯Novavax签署预购协议,购买该公司的重组蛋白疫苗,并有望在今年年底前送达新加坡。这款疫苗目前仍在进行第三期临床试验。
诺瓦瓦克斯公司生产的是一款重组蛋白疫苗,采用蛋白质亚基(protein subunit)和重组病毒糖蛋白纳米颗粒(recombinant nanoparticle)技术,和目前人们熟悉的乙型肝炎或破伤风疫苗原理相同,让人体免疫系统对疫苗中的蛋白质产生反应。

诺瓦瓦克斯6月14日发声明表示,公司在美国和墨西哥119个地点对2万9960人进行研究,以评估疫苗的效能、安全性,以及免疫原性。
疫苗对预防中度和重症冠病的效能达100%,整体效能为90.4%。公司计划今年第三季向美国和欧洲的监管局申请使用。
新加坡国立大学苏瑞福公共卫生学院院长张毅颖教说:“增加疫苗的种类是为确保疫苗来源多元化。更重要的是,这不是一款mRNA疫苗,能保护不适合接种mRNA疫苗的人。临床数据显示这款疫苗的效能很高,和辉瑞与莫德纳等mRNA疫苗相近。”























评论