5天见效的“神药”来了?美国新冠肺炎口服药物售价超成本40倍
本文来源:时代周报 作者:马欢
首款针对新冠肺炎病毒的口服药物或将到来。
当地时间10月11日,美国制药企业默克(Merck & Co.)表示,他们已向美国食品药品监督管理局(FDA)申请抗新冠肺炎口服药“莫那比拉韦(Molnupiravir)”的紧急使用授权(EUA)。如申请获批,莫那比拉韦将成为首款针对新冠肺炎的口服抗病毒药物。
莫那比拉韦由默克和里奇巴克生物医药公司(Ridgeback Biotherapeutics LP)联合研发。默克公布的临床数据显示,莫那比拉韦能够让新冠肺炎轻度至中度患者住院率和死亡率减半。对此,白宫顾问、美国国家过敏症和传染病研究所所长安东尼·福奇表示,默克的临床数据“是非常好的消息”,但他要求FDA在审查这些数据前必须谨慎行事。
有美国媒体认为,该款口服药物具有开创性意义,因为其不仅可以缓解症状,加速恢复,减轻医院医疗负担,有助于遏制疫情在卫生系统较薄弱的贫穷国家爆发,还可以为应对疫情提供一种双管齐下的方法:通过口服药物治疗和通过接种疫苗预防新冠肺炎肺炎。
目前,除了美国外,新加坡、日本、韩国、澳大利亚等多国都加入了这款“神药”的抢购行列。
美国知金融博客ZeroHedge表示,这款药物若获得批准,即将成为 “有史以来最赚钱的药物” 之一。财经网站Quartz更预计,截至2021年年底,莫那比拉韦能会为默克公司及其合作伙伴Ridgeback带来高达70亿美元的收益。

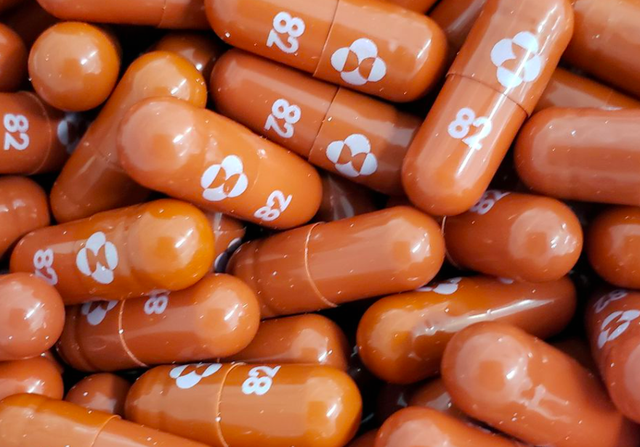
莫那比拉韦(图源:美国默克公司)
“神药”效果几何
事实上,莫那比拉韦是一款老药,它原本用于治疗流感,但在后来的体外细胞学实验中发现,它对SARS和MERS等冠状病毒亦有作用。在新冠肺炎疫情暴发后,默克公司便开始研究其抗击新冠肺炎病毒的疗效。
作为广谱抗病毒药物,莫那比拉韦的作用原理是阻止病毒的复制,它能有效令新冠肺炎病毒在复制期间出现大量错误,促成“致死突变”(Lethal mutagenesis)让病毒复制失败,继而抑制病毒增长。
莫那比拉韦最大的优势就是它是小分子口服药物,每12小时口服一粒,患者在家服用即可,避免了传播病毒的风险。相比之下,吉利德科学公司的瑞德西韦和单克隆抗体疗法,都需要在医院通过静脉注射给药。而且,口服药物不像疫苗那样必须冷藏,因此更易于常温运输和储存。
在10月1日,默克公司还公布了莫那比拉韦的Ⅲ期临床数据,在初次接受治疗的775名患者中,每天服用莫那比拉韦两次、连续服用5天的人,在其接受治疗的29天内的住院率为7.3%,且死亡率为零。相比之下,使用安慰剂的患者组住院率为14.1%,并有8人死亡。从有效性上看,莫那比拉韦将轻度/中度新冠患者的住院死亡率降低50%,取得了显著的治疗效果。安全性数据则显示,莫那比拉韦的副反应发生率(12%)与安慰剂组(11%)相当。
默克方面称,病毒测序表明,莫那比拉韦对所有新冠肺炎变种病毒都有效,包括德尔塔毒株。
目前,每名患者为期5天的莫那比拉韦疗程的费用约为700多美元(约合人民币4519元),是单克隆抗体治疗费用的三分之一。默沙东方面表示,莫那比拉韦安全、耐受性好、价格合理、易于使用的,能直接对抗病毒。
“莫那比拉韦今后一定能够在抗击全球新冠大流行中成为重要药物,如果能够得到批准,也会对现有的新冠大流行状况产生深远影响。”默克公司CEO戴维斯说道。

图源:路透社
争议不小
虽然莫那比拉韦的疗效令人鼓舞,但其带来的争议也不少,甚至被质疑是在赚取暴利。
哈佛公共卫生学院和伦敦国王学院医院药物定价专家发布的一份报告表示,莫那比拉韦生产成本仅为17.74美元(约合人民币115元),但默克公司向美国政府收取的费用却是生产成本的40多倍。
国际医疗救援组织“无国界医生”官员利娜•门加尼亦呼吁,世界需要廉价的非专利药物。
面对暴利的质疑,默克公司已承诺向全球提供莫那比拉韦,并与5家生产仿制药的印度公司签订许可协议,允许他们向全球100多个中低收入国家生产和销售莫那比拉韦。按照这份协议,印度仿制药公司计划将此药5天疗程价格定在约12美元(约合人民币77元)左右。
但对于向美国和其它许多中高等收入国家,默克方面表示,药价会根据市场情况决定。
另外一个争议则来自于药物本身,据《巴伦周刊》报道,部分科学家担心这种药物可能会导致癌症或先天缺陷——因为莫那比拉韦抑制病毒的方法可能会在体内肆虐。

莫那比拉韦(图源:美国默克公司)
埃默里大学儿科教授兼生化药理学主任雷蒙德·希纳齐在研究后表示,莫那比拉韦用来杀死新冠病毒的方法存在潜在危险,如果这种情况发生在接受治疗的患者的细胞中,理论上可能会导致癌症或先天缺陷。
希纳齐认为,在没有更多数据支持的情况下,莫那比拉韦不应该用于年轻人,尤其是孕妇。
对此,默克公司方面回应道:已经对动物进行了 “广泛的测试”,并表示这应该不是问题。
“目前研究的全部数据表明,莫那比拉韦在哺乳动物系统中没有致突变性或基因毒性。”默克公司发言人说。但该公司截至目前仍尚未公布其动物研究的任何数据,一些科学家们认为,需要长期研究才能证明该药物是真正完全安全的。
虽然尚存争议,但却并不影响莫那比拉韦的“抢手”程度。
早在今年6月,默克公司便与美国政府达成了一项价值12亿美元的供应协议。根据协议,一旦莫那比拉韦获得FDA紧急使用授权或批准,默克公司将提供170万个疗程的治疗。
此外,还有多个国家也加入了抢购莫那比拉韦的行列。
据路透社报道,澳大利亚已经提前预定购买30万剂的莫那比拉韦,韩国也已经通过合同预订了2万剂。10月6日,默克宣布与新加坡政府签订采购合同。其他国家如日本、泰国和马来西亚均表示,正与默克公司磋商采购事宜。
欧洲药品管理局也表示,将考虑开始对莫那比拉韦进行快速审批。
默克指出,预计到2021年底将生产1000万个疗程的莫那比拉韦,更多剂量则定于2022年投产。
还有哪些口服药物在“路上”
除了莫那比拉韦,目前多国药厂均在研发新冠口服药物,并已经有一些药物走在研发前列。
首先是美国辉瑞公司研发的新冠口服药PF-07321332,它是一种蛋白酶抑制剂,针对新冠病毒具有抗病毒活性。辉瑞在9月27日发布的新闻稿宣布,PF-07321332将展开中至后期临床试验。
瑞士罗氏也在研发一款代号AT-527的针对新冠病毒的口服抗病毒药物。今年6月,罗氏公司发布了AT-527的II期数据,表现虽不如莫那比拉韦,但罗氏表示,该药物未来有潜力用作暴露后的预防性治疗。同时,罗氏在临床设计上与默克也采取了差异性方案,以症状开始缓解时间作为主要目标,预计今年年内将有Ⅲ期数据公布。
9月底,日本盐野义制药宣布,他们正在研发的新冠口服药物s217622也进入了最后阶段的临床试验。与辉瑞公司的口服药相同,s217622也是一种蛋白酶抑制剂。I期临床试验于今年7月在日本开始,目前正在进行针对轻度COVID-19或无症状SARS-CoV-2感染患者的II期和Ⅲ期临床试验。
中国也有药厂在研发新冠口服药物。10月4日,开拓药业发布公告称,其研发的一款AR(雄激素受体)拮抗剂口服药物普克鲁胺Ⅲ期全球多中心临床试验已于10月1日在美国的临床中心完成首例患者入组及给药。该公司表示,临床试验计划已在中国、菲律宾及巴西等14个国家的医疗中心展开。开拓药业的相关研究称,普克鲁胺通过抑制雄激素受体功能,进而阻断新冠肺炎病毒进入宿主细胞。


















评论