重磅解读:近期干细胞研究领域这10项重要研究成果
近日,来自加利福尼亚大学等机构的科学家们通过研究能够成功维持鸡蛋中的胚胎干细胞并阐明了胚胎干细胞的命运,该研究或为科学家们研究干细胞多能性和进化发育的生物学特性提供新的见解。那么近期科学家们在干细胞研究领域还有哪些重要研究成果呢?本文中,小编整理了相关研究,分享给大家!

ipsC疫苗注射剂控制疗法施行后,肿瘤引流淋巴结中CD8+ T细胞激活状态和T细胞亚群频率之间的差异。
图片来源:Xiaoming Ouyang,et al. Stem Cell Reports (2021). doi:10.1016/j.stemcr.2021.04.004
【1】Stem Cell Rep:基于诱导多能干细胞的疫苗策略或有望产生强大的抗胰腺癌潜能
doi:10.1016/j.stemcr.2021.04.004
胰腺导管腺癌(PDAC)是美国癌症相关死亡的第四大原因,在过去几十年里PDAC患者的5年生存率一直处于个位数的水平;截止目前为止,手术依然是治疗这种疾病最有效的方法;然而,仅有大约10%的患者能够在早期阶段被诊断出来,从而及时接受手术来移除肿瘤。尽管科学家们在免疫检查点抑制剂研究领域取得了一定的成功,但PDAC仍然对这些药物制剂具有一定的耐受性,这就使得这类癌症因其间质促纤维增生、缺乏效应T细胞及较低的突变负担而成为了一种难治性的癌症。
诱导多能干细胞(ipsCs)和癌症拥有细胞的相似性和转录组特性;日前,一篇发表在国际杂志Stem Cell Reports上题为“Antitumor effects of ipsC-based cancer vaccine in pancreatic cancer”的研究报告中,来自斯坦福大学等机构的科学家们通过研究深入探究了使用诱导多能干细胞中的非突变肿瘤相关蛋白质来作为开发PDAC疫苗基础的可能性。我们都知道,适应性免疫系统能够识别并对非突变肿瘤相关的抗原(TAAs)产生反应,FDA批准的名为Provenge的治疗性癌症疫苗就能作为一种基于TAA的疫苗;研究人员指出,诱导多能干细胞和癌细胞共享着基因表达谱,对iPSC细胞系和癌细胞系的RNA测序数据进行聚类分析后,研究者发现其二者共享着上调基因,这种被称为ipsC-癌症特征性基因的特殊基因能被多潜能细胞群高度表达,但在体细胞组织中仅会轻微或根本不表达。
综上,本文研究结果支持了在PDAC临床前和临床模型中进行iPSC疫苗接种的进一步研究,同时ipsC疫苗还适用于在拥有较低突变负担的其它癌症类型中的研究;当然,后期研究人员还希望能通过深入研究揭示是否ipsC癌症疫苗在患者机体中是安全且有效的,同时还能有效抑制肿瘤生长和再度生长,并能帮助清除已经形成的肿瘤。
【2】Nat Commun:科学家发现影响血液干细胞中特殊基因表达的关键元件
doi:10.1038/s41467-020-20282-1
基因转录通常会被启动子和调节元件(比如增强子和沉默子)之间的染色质环来进行调节,不同的转录因子(TFs,transcription factors)能够与这些调节元件结合,并以一种细胞类型特异性的方式来调节启动子-增强子环。尽管其在控制基因表达方面发挥着重要作用,但转录因子如何促进启动子-增强子环,目前研究人员尚不清楚。
CCCTC结合因子(CTCF)是一种维持染色质间相互作用的重要因子,然而研究人员并不清楚调节其与染色质结合之间的分子机制。生物体能通过一种生物化学过程错综复杂网络来保持活力并维持健康状况,这些过程在应对环境改变方面往往具有显著的可塑性,但有时其也会出错,医学研究领域的一个关键原则就是了解这些途径从而更加有效地治疗疾病。日前,一篇发表在国际杂志Nature Communications上题为“ZNF143 mediates CTCF-bound promoter–enhancer loops required for murine hematopoietic stem and progenitor cell function”的研究报告中,来自新加坡国立大学等机构的科学家们通过研究发现了一种特殊的分子开关,其或能控制细胞开启基因的表达和关闭的过程,这一过程能够确保细胞正确且充分地执行其在体内的指定任务。
本文研究或能帮助改善科学家们对正常干细胞发挥功能机制的理解,同时也能帮助阐明某些疾病的发病机制。Tenen教授说道,基于本文研究结果,后期我们将有望理解CTCF-DNA之间结合和基因表达的调节性机制,而这对于调查人类的发育障碍和癌症发生意义重大;后期研究人员还将继续深入研究相关蛋白质的分子结构来进一步阐明多种人类疾病的发病机制。综上,ZNF143-CTCF结合启动子增强子环或能调节基因表达的模式,这对于维持小鼠造血干细胞和祖细胞的功能及完整性至关重要,此外,研究人员还发现了基因调节的一个共同特征,即ZNF143是CTCF结合启动子增强子环的关键因子。
【3】Stem Cells:衰老生态位可使造血干细胞的“返老还童”?
doi:10.1002/stem.3372
造血干细胞的衰老可引起与衰老相关的白血病以及相关的免疫重构。在体外使用Cdc42(可导致造血干细胞衰老)活性特异性抑制剂治疗衰老的造血干细胞后,将其移植到年轻的受者体内后仍能保持活力。在该研究中Novella Guidi教授团队确定了衰老生态位对体外再生衰老星状细胞功能的影响,结果表明,衰老生态位抑制了体外再生造血干细胞的功能,这至少在一定程度上与衰老生态位中发现的低水平细胞因子骨桥蛋白有关,这为我们解决衰老生态位对衰老造血干细胞在体内持续恢复功能的影响提供了思路。
本研究的目的是确定衰老生态位是否可能影响新陈代谢的造血干细胞的年轻样功能。研究人员将年老供体(Ly5.1+)的200个造血干细胞在体外+/酪蛋白处理16小时,然后移植到年轻(Y)、年老(A)或年轻骨桥蛋白(OPN)敲除(KO)受体(Ly5.2+)小鼠中。B:年轻、年老OPN KO受体(Ly5.2+)小鼠外周血总白细胞(PB)中老年人供体(Ly5.1+细胞)+/酪蛋白的频率。C:衰老B细胞+/酪蛋白的频率。D:衰老T细胞+/酪蛋白。E:年轻、年老的OPN KO受体(Ly5.2+)小鼠PB中供体来源的Ly5.1+细胞中的老年髓系细胞+/酪蛋白。F:年轻、老年和年轻OPN KO受体(Ly5.2+)小鼠供体来源的Ly5.1+LSK细胞中老年LT-HSCs +/ CASIN 在骨髓的频率。数据基于每组3只受体小鼠的5次重复实验。
总之,年轻化的老年造血干细胞移植到年轻受体后,其持续的年轻功能依赖于干细胞内在和干细胞外在因素(生态位/微环境)的结合。当再生的老年造血干细胞被移植到年轻小鼠体内时,其衰老的一些特征又会回到衰老的表型。对于某些表型来说,这可能是由于老年生态位中骨桥蛋白水平的降低。因此,为了在体内恢复衰老的造血干细胞,需要考虑生态位对再生造血干细胞的影响。
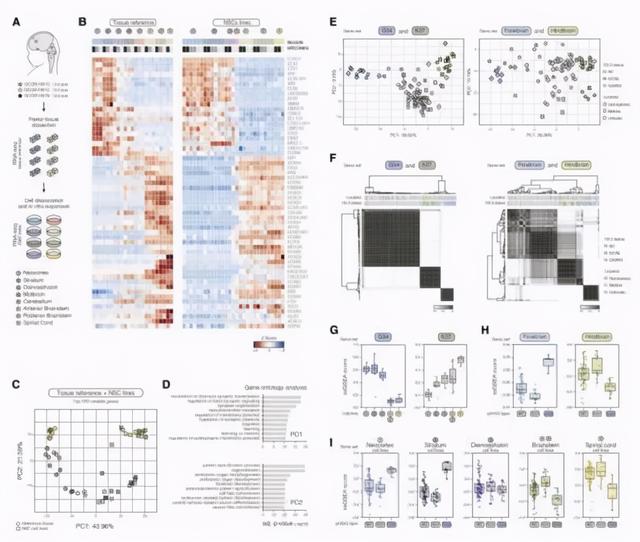
人胚胎神经干细胞培养保留了区域特征,并概括了PHGGs的转录特征。
图片来源:doi:10.1016/j.stem.2021.01.016
【4】Cell Stem Cell:科学家揭秘人类神经干细胞的区域特性
doi:10.1016/j.stem.2021.01.016
来自英国爱丁堡大学再生医学中心和再生与修复研究所Steven M Pollard 教授带领团队,在Cell 子刊《Cell Stem Cell》杂志上发表了题为“Regional identity of human neural stem cells determines oncogenic responses to histone H3.3 mutants”的研究论文。
前期研究表明,使用组织衍生细胞模型克服了基于胚胎干细胞(ESC)或诱导多能干细胞(ipsC的模型相关的缺点,这些模型变幻无常,需要冗长的分化方案,并导致异质混合物细胞类型。值得注意的是,除了解剖H3.3-癌组蛋白的作用之外,该研究团队的主要胎儿NSC系的确定的起源和身份也可以促进在特定CNS区室中出现的其他儿科肿瘤的建模,例如成神经管细胞瘤或室管膜瘤。鉴于此,该研究团队和其他人正在开发大量跨越不同时间和空间特征的人类胎儿NSC细胞系,这些细胞系应该能够对不同的脑肿瘤驱动因子进行功能性解剖,并提供给研究界。进一步利用该研究团队的同基因模型,研究人员能够在相关细胞环境中获得对H3.3-G34R作用模式的分子见解。通过mRNA分析和组蛋白翻译后修饰作图的组合,该研究团队观察到H3.3-G34R不会诱导普遍的转录或表观遗传变化,而是在已经高度表达的基因上起作用,包括关键的前脑NSC转录因子。这些发现与报道的H3.3-K27M在中线pHGG和小儿肉瘤中存在的其他H3.3驱动突变中的作用形成鲜明对比,其中癌基因似乎引起表观遗传景观的广泛重置。
总之,该研究团队的研究结果表明,与人类神经祖细胞区域特征相关的细胞内在程序为不同的H3.3 癌组蛋白提供了独特的脆弱性,这可能解释了儿童高级别胶质瘤的独特解剖分布。现在将需要进一步的工作来充分剖析为什么区域祖细胞状态对每个H3.3突变具有不同的敏感性,以及是否可以将维持前脑和后脑身份的机制作为治疗目的的目标。该研究团队希望,对关键靶细胞群的这种鉴定以及潜在的易感性机制,可能最终导致针对这种破坏性疾病的更有效疗法。
【5】Stem Cell Res:胞外特殊的层粘连蛋白或能调节多能干细胞的造血潜能
doi:10.1016/j.scr.2021.102287
诱导多能干细胞(iPSCs)的神奇之处在于其能够大量增殖并分化为所有类型的细胞,以便最初少量的iPSCs能够用于制造大量的机体细胞;然而,一些细胞已经被证明要比其它细胞更加容易产生和制造,而这对于ipsCs的研究转化到临床疗法中的成本和花费或许具有重大影响;近日,一篇刊登在国际杂志Stem Cell Research上题为“Extracellular laminin regulates hematopoietic potential of pluripotent stem cells through integrin β1-ILK-β-catenin-JUN axis”的研究报告中,来自日本京都大学等机构的科学家们通过研究发现,一种广泛存在于人类机体中并用于iPSCs疗法的特殊分子—层粘连蛋白(laminin)或许会影响ipsCs的造血分化。
研究人员利用LM511-E8将iPSCs分化出了多种类型血细胞,包括他们给患者机体中输注的血小板等,这种分化的基础是研究者10多年前发现的Sac方法。Sac方法主要是针对iPSCs的造血分化,其能够遵循原条结构、中胚层、血管内皮的状态来产生造血祖干细胞。换句话说,这种方法能试图重现天然的造血作用从而产生造血祖细胞,而造血祖细胞是一种所有其它血细胞都能够衍生的细胞类型。然而这种方法并非没有缺陷,研究人员注意到,相比ipsCs的数量,他们所获得的造血祖细胞的数量相当少。
综上,胞外层粘连蛋白支架或能通过在未分化阶段激活ITGB1-ILK-β-连环蛋白-JUN轴来调节造血干祖细胞的分化潜能;而低浓度的LM511-E8和修饰后的造血干祖细胞-Sac方法联合后或能获得较高的造血祖细胞产量以及更高的最终造血率,这就为从一般的造血干祖细胞获得分化的造血细胞提供了一种非常有用的方案或步骤。
【6】Nature子刊:科学家揭秘造血干细胞的造血机制
doi:10.1038/s41467-021-22053-y
表观遗传调节因子ASXL1、TET2和DNMT3A的体细胞突变在造血干细胞中被反复检测到。小鼠中TET2或DNMT3A的缺乏增强了LT-HSCs的自我更新,这表明TET2和DNMT3A的突变诱导造血细胞的克隆扩增,导致人类的克隆性造血。相比之下,小鼠中的ASXL1突变减少了HSCs的数量和功能。
基于此,来自日本东京都港区东京大学医学研究所细胞治疗学系的Makoto Suematsu 教授,带领团队将关于造血干细胞的相关研究以“Mutant ASXL1 induces age-related expansion of phenotypic hematopoietic stem cells through activation of Akt/mTOR pathway”为题,于2021年3月23日在线发表在《Nature Communications》杂志上。该研究团队观察到年龄相关的造血表型增强,包括贫血、骨髓偏向性分化、低细胞骨髓和表面标记物定义的LT-HSCs在老年ASXL1-MT KI小鼠中的扩增。这些表型通过抑制Akt/mTOR途径得到部分挽救,表明ASXL1-MT诱导的Akt/mTOR途径的激活与造血系统的增强老化有关。此外,RNA-序列分析显示ASXL1-MT促进年龄相关模式的基因表达。这些结果表明ASXL1-MT可能通过激活Akt/mTOR途径促进HSC衰老。
总之,该研究团队表明ASXL1-MT与BAP1合作,以表观遗传学独立的方式激活Akt/mTOR途径。活化的Akt/mTOR途径导致PlT-HSC在老化过程中异常膨胀,占据HSc室。Akt/mTOR信号过度活跃还会导致线粒体激活、ROS过度产生、DNA损伤增加以及随后的造血干细胞功能障碍。pLT-HSCs的扩张以及ASXL1突变引起的DNA损伤的增加可导致CH的发展,导致造血系统恶性肿瘤的继发突变。Akt/mTOR途径的药理学抑制可能为携带ASXL1突变的先天性心脏病患者的预防性干预铺平道路。
【7】PNAS:单细胞水平揭示造血干细胞扩增的动态图谱
doi:10.1073/pnas.2015748118
在脊椎动物中,胚胎发生期间产生的最早确定的造血干细胞和祖细胞(HSPC的)可以产生多种血液谱系并表现出自我更新的属性。为建立HSPC池,新生的HSPC将首先迁移到临时性的造血器官,称为胎肝(FL,在哺乳动物)或尾造血组织(CHT,在斑马鱼)。临床上,体外HSPC扩展是获得足够的可移植HSPC的可行方法,但在技术上仍然具有挑战性。因此,解码造血器官内HSPC扩展的复杂调控机制至关重要。
基于此,中科院动物研究所刘峰课教授团队在《PNAS》杂志上发表题为“A single-cell resolution developmental atlas of hematopoietic stem and progenitor cell expansion in zebrafish ”的研究论文。该研究团队揭示了人类胎儿肝脏与斑马鱼CHT之间发育性造血的保守性和差异性。在这项研究中,该研究团队将scRNA-seq与功能测定结合使用以解码发育中的CHT。首先,该研究团队解决了胎儿HSPC异质性,表现为谱系启动和代谢基因签名。该研究团队进一步分析了非造血生态位成分和HSPC之间的细胞相互作用,并鉴定了内皮细胞特异性因子Gpr182,随后对其在促进HSPC扩展中的作用进行了实验验证。最后,该研究团队揭示了人类胎儿肝脏与斑马鱼CHT之间发育性造血的保守性和差异性。该研究团队的研究为胎儿HSPC的发展提供了宝贵的资源,并为建立体外HSPC扩展的支持提供了有利的研究基础。
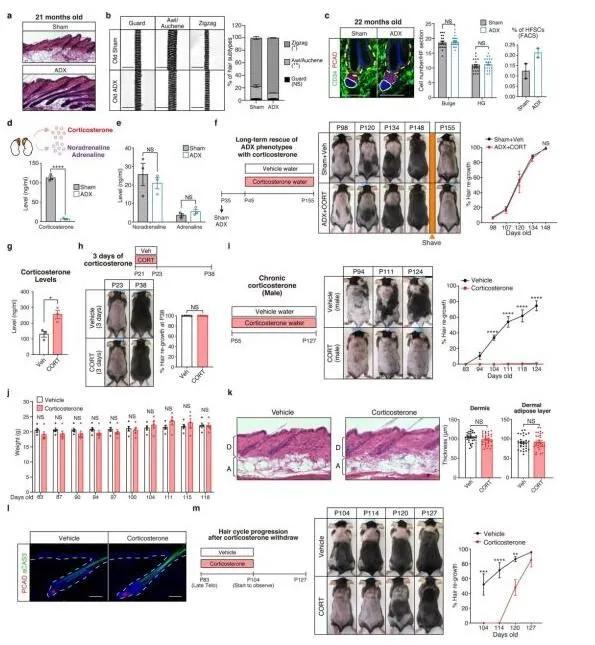
皮质酮可恢复ADX小鼠正常的毛发周期进展。
图片来源:Nature, 2021, doi:10.1038/s41586-021-03417-2
【8】Nature:放轻松也许可以治疗脱发!新研究揭示慢性压力调控毛囊干细胞机制
doi:10.1038/s41586-021-03417-2
当美式橄榄球四分卫Aaron Rodgers在一个赛季糟糕的开局后告诉球迷们放松一下时,他几乎不知道自己这也是给出头发护理建议。在COVID-19大流行一年后,他的建议现在特别有用。约有四分之一感染新冠病毒的人在症状发生六个月后出现脱发,这可能是由于感染和恢复的折磨导致的全身性冲击。长期以来,慢性压力(也称为慢性应激)与脱发有关,但是将压力与毛囊干细胞功能障碍联系起来的内在机制尚不清楚。美国哈佛大学的Ya-Chieh Hsu博士及其团队在一项针对小鼠的新研究中揭示了这种联系。相关研究结果于2021年3月31日在线发表在Nature期刊上,论文标题为“Corticosterone inhibits GAS6 to govern hair follicle stem-cell quiescence”。
文章中,研究人员首先通过外科手术将肾上腺从小鼠身上移除,以便测试它在调节毛发生长中的作用,其中肾上腺产生压力激素(也称为应激激素)并是一种重要的内分泌器官。这些移除肾上腺的小鼠(该团队称为ADX小鼠)的毛囊的休止期要短于对照组(少于20天,而对照组为60~100天),毛囊参与毛发生长的频率大约是对照组的三倍。通过给ADX小鼠喂食皮质酮(一种通常由小鼠肾上腺产生的应激激素),他们能够抑制这种频繁的毛发生长并恢复正常的毛发周期。有趣的是,当他们不可预知地对正常小鼠施加各种轻度压力达九周之久时,他们观察到皮质酮水平升高,并伴随毛发生长减少,这支持了肾上腺在慢性压力下产生的皮质酮抑制毛发生长的想法。
为了了解真皮乳头如何将这种压力信号传递给HFSC,Hsu团队对在真皮乳头中表达的信使RNA(用作蛋白表达的模板)进行了分析。这表明一种称为GAS6(growth arrest-specific 6)的分泌蛋白可以作为候选分子信使。确实,使用腺病毒载体(基因治疗中的一种常用工具)将GAS6递送到皮肤中不仅刺激了正常小鼠的毛发生长,而且还恢复了慢性应激或皮质酮喂食期间的毛发生长。
【9】Nature子刊:揭示一种化学物混合物可产生大量的肌肉干细胞
doi:10.1038/s41551-021-00696-y
在一项新的研究中,来自美国加州大学洛杉矶分校的研究人员鉴定出一种化学物混合物,它能够大量地产生可以自我更新并可产生所有类型骨骼肌细胞的肌肉干细胞。这一进展可能导致开发基于干细胞的疗法,以治疗因受伤、年龄或疾病而导致的肌肉损失或损伤。相关研究结果近期发表在Nature Biomedical Engineering期刊上,论文标题为“Skeletal muscle regeneration via the chemical induction and expansion of myogenic stem cells in situ or in vitro”。
肌肉干细胞在人的一生中负责肌肉生长、修复和受伤后的再生。在完全成长的成年人中,肌肉干细胞是静止的---它们一直处于非活动状态,直到它们被要求通过自我复制和产生修复受损组织所需的所有细胞类型,对损伤作出反应。但是,随着人们年龄的增长,这种再生能力会下降;它也会因外伤和杜兴氏肌肉营养不良等遗传性疾病而受到损害。研究者表示,基于肌肉干细胞的疗法在改善肌肉再生方面有很大的前景,但是目前产生患者特异性肌肉干细胞的方法可能需要几个月的时间。”
Li和他的同事们发现了这种化学物混合物---根茎提取物forskolin和小分子RepSox的组合---可以在10天内有效地产生大量的肌肉干细胞。在小鼠研究中,这些研究人员展示了这种化学物混合物可能用作疗法的两种潜在的途径。第一种方法使用在皮肤中发现的称为真皮肌原细胞(dermal myogenic cell)的细胞,它们有能力成为肌肉细胞。Li及其团队发现,用这种化学物混合物处理真皮肌原细胞,可促使它们产生大量的肌肉干细胞,然后所产生的肌肉干细胞可被移植到受伤组织中。
【10】Cell Stem Cell:新发现!核糖体装配对于造血干细胞的再生非常重要!
doi:10.1016/j.stem.2021.02.008
近日,一项刊登在国际杂志Cell Stem Cell上的研究报告中,来自费城儿童医院等机构的科学家们通过研究识别出了通过核糖体组装进行造血干细胞(HSC,hematopoietic stem cell)再生的关键基因,核糖体是细胞中的蛋白质制造工厂,其能将mRNA序列转化成为氨基酸序列;本文研究结果强调了合适的蛋白质装配对于干细胞再生的重要性,并识别出了潜在的靶点有望帮助开发治疗核糖体病变(ribosomopathies)及诱发骨髓衰竭的儿童障碍的新型疗法。
研究者Wei Tong表示,尽管此前研究结果表明,影响核糖体装配的突变与参与骨髓功能障碍的人类疾病的发生直接相关,但我们并不清楚造血干细胞中核糖体装配被调节的分子机制以及其是如何诱发疾病发生的。文章中,研究人员识别出了能阻止核糖体在哺乳动物细胞中进行合适装配进行诱发造血干细胞不足的分子机制,这或许有望未来开发新型的疾病干预策略。
研究人员还发现,在Hectd1缺失的造血干细胞中敲除ZNF622基因或能恢复大亚基和小亚基进行适当结合的能力,从而就会恢复蛋白质的合成和造血干细胞的产生。最后研究者Tong说道,相关研究结果不仅强调了蛋白质降解、核糖体装配以及干细胞产生之间的关系,而且还揭示了敲除ZNF622从而来恢复机体正常的骨髓功能的重要性,这对于儿童发育至关重要。后期研究人员还希望进一步研究将这种机制作为一种潜在的靶点来帮助开发治疗相关疾病的新型疗法。
来源:细胞 微信公众号


















评论