无自主研发专利,却成资本宠儿,融资近30亿的云顶新耀能否登港

作者 | 刘芬
编辑 | 李红梅
来源 | 风云资本界
2020年1月,原计划港股IPO的天境生物在美国纳斯达克成功上市。康桥资本持股38.9%,是其第一大股东。赴美上市前,天境生物已获得弘毅资本领投的2.27亿美元C轮融资,是当时中国创新药领域C轮最大的融资。
2020年6月,康桥资本孵化的另一家生物制药企业云顶新耀,获得3.1亿美元C轮融资,打破了这一最大融资记录,引得市场瞩目。一个月后,这家企业又趁势向港股发起进击。
7月19日,云顶新耀(Everest Medicines Limited)向港交所正式递交了上市申请。
招股书显示,云顶新耀是一家临床后期生物制药公司,业务包括全球同类首创或同类最佳疗法的许用、临床开发及商业化,以解决大中华及亚太区其他新兴市场尚未得到满足的医疗需要,产品管线覆盖了肿瘤、免疫性疾病、感染性疾病、心肾疾病4大领域。
风云资本界注意到,该公司成立于2017年,至今尚未盈利。
财报数据显示,截至2020年3月31日,公司现金及现金等价值物为7350万元。2018年、2019年及2020年第一季度,经营亏损净利额分別为1.27亿元、1.76亿元、1.51亿元。

(图片来源:招股书)
云顶新耀解释称,绝大部分亏损是由于研发计划产生的成本、运营相关的一般及行政成本。随着开展开发有关的若干活动,公司预计亏损未来将增加。
不过,得益于港交所在2018年4月发布的上市新规,允许未有收益或盈利的生物科技企业在香港主板上市。诺诚健华(09969.HK)、开拓药业(09939.HK)、康方生物-B(09926.HK)和沛嘉医疗-B(09996.HK)这些报告期内巨亏的企业,已于上半年顺利叩开港股大门,沛嘉医疗-B更是在上市首日大涨67.97%。
对于生物制药公司而言,未盈利前,企业的持续经营能力在上市过程中易受到质疑。核心产品和研发团队的实力如何?是否拥有核心产品的技术专利权?是否具备持续研发的能力与资金?这些都是上市审核比较看重的问题。
云顶新耀在这些方面表现如何呢?
不做自主研发
风云资本界注意到,该公司目前并不从事新候选药物的自主研究或发现,主要通过获得许可协议的模式开发其他方已发现的候选药物。大部分引进的授权产品及候选产品为全球伙伴的顶级资产,倾向选择已完成临床概念验证阶段的候选产品。
招股书显示,自2017年7月起,云顶新耀已评估百项资产,从美国及欧洲的生物制药公司获得了八款候选药物的授权许可,每款在亚太地区均具有临床未满足需求和数十亿元的销售市场潜力。
其中,eravacycline及sacituzumab govitecan两款产品已分別获美国食药监局批准NDA(新药申请)及BLA(生物制剂许可申请),有六款产品正在中国进行或步入注册性试验。
但是,除获准在新加坡上市的eravacycline外,其他候选药物均未获准在中国或云顶新耀已获得许可权力的任何其他司法权区上市。当前阶段,公司仍将大量工作重点放在现有候选产品的持续临床试验、潜在批准及商业化上。
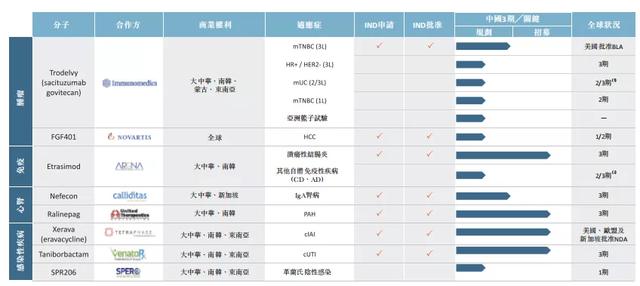
(图片来源:招股书)
云顶新耀在招股书中称,为开发新候选药物,公司已组建一支高级领导团队,有多次成功开发新型疗法、引领公司在不断转变的监管环境中前进,以及在中国商业化创新药物的往绩。
信息显示,由朱煦担任感染性疾病首席医学官,她曾是拜耳医药保健公司一般内科抗感染治疗领域的临床新药研发负责人;朱正璎担任内科首席医学官,她曾是山东罗欣药业的首席医学官及业务开发主管;时阳担任肿瘤科首席医学官,她曾在默克雪兰诺(北京)医药任临床开发主管。
云顶新耀首席执行官、医学博士薄科瑞在6月接受采访时曾说道,云顶新耀有120个员工,其中有3个CMO(即首席医学官),一般企业只会有一个CMO。全部员工分配在三个项目里,分别是肿瘤团队、抗生素团队、心肾团队。现在有4个临床项目正在推进中,今年还会再有2个临床项目。
170余项专利背后的“依赖”
众所周知,若无法就候选药物完成临床开发、获得监管批文并将其商业化,或若在此过程中遇到重大延误,业务将受到重大损害。而对于制药公司而言,许可协议、专利是成功与否的重要因素。
招股书显示,截至2020年6月30日,云顶新耀覆盖的地域范围取得超过170项专利及待批专利申请许可。但是,开发候选药物必不可少的若干专利权及其他知识产权依赖于第三方的许可及转授许可。
云顶新耀称,公司并不拥有该等候选药物相关知识产权,因此权力受持续性影响,且须遵守协议条款。若许可遭终止,竞争对手可自由开发相同的产品、就有关产品寻求监管批文或上市。此外,许可协议可能并无权力控制公司药物的专利及专利申请的准备、提交、申请、维持、实施及保护。
与此同时,许可人可能倚赖第三方的资金、资源或知识产权,导致许可人并非云顶新耀获许可专利的唯一拥有人。其他第三方将有关专利授予云顶新耀的竞争对手,或许可人未来不能从第三方获得足够权利及许可,都可能成为云顶新耀的业务上的不确定因素。
风云资本界简单估算八种候选药物的授权时间后发现,不同产品在不同地区的到期时间略有差异。比如,涉及Eravacycline的专利权,一般在2025年至2029年间到期;涉及FGF401的专利权,一般在2034年至2037年到期。
据招股书披露的授权内容显示,以Eravacycline为例,专利期以逐个国家及逐项产品计而延续,自于某个国家首次作商业销售开始,直至在该国家包含有效申索条文的最后到期许可专利到期,在该国的Eravacycline产品独家营销或监管权到期,或于国家的Eravacycline产品首次商业销售起计10年。
根据授权协议,在协议期内以及终止协议期后三年內,公司不可在许可地区之外就许可适应症以外的任何适应症开发或商业化Eravacycline或相关产品。
资本“宠儿”
事实上,这些许可协议的关键条款还包括云顶新耀须向许可人支付的款项。
招股书显示,其中可能包括签署协议时的预付款、里程碑付款以及按许可权涵盖产品的年度销售净额的指定百分比计算的特许权使用费。截至最后实际可行日期,云顶新耀已经为现有的八种候选药物合计支付14.9亿元的预付款及里程碑付款。
云顶新耀在招股书中谈及风险时称,若获得相关批文,最后销售获得的利润将因支付特许权使用费而减少。即使候选药物未曾获准销售,或无法将其商业化,公司也可能面临合约义务须支付大量款项。此外,在获得监管批文或将其商业化前,候选药物里程碑款项或其他非特许权使用费亦可能已到期,公司可能并无足够资金支付该到期款项。
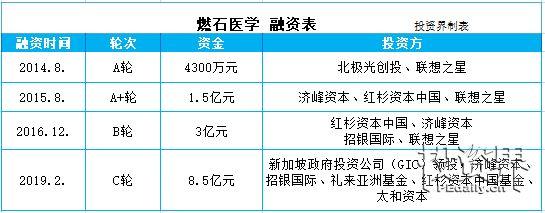
不过,风云资本界注意到,云顶新耀自成立以来备受资本青睐。2017年和2018年,云顶新耀分别获得5000万美元、6000万美元融资,2020年6月,又获得3.1亿美元C轮融资,前后累计融资4.2亿美元(约人民币29.25亿元)。这些私募融资无疑为云顶新耀解了燃眉之急。细数其投资方,其中不乏贝德莱(BlackRock)、德诚资本、骏利亨德森投资等明星资本。
与此同时,公司控股股东为亚洲最大医疗保健专门投资企业CBC,上市前持有62.48%股权,康桥资本拥有CBC集团73%股份。
云顶新耀董事长兼康桥资本首席执行官傅唯曾表示,“实力雄厚的投资者的加入,不仅彰显了公司出色的早期成果,又体现了投资者对云顶新耀成长为地区领先的创新药物平台公司的信心”。
此次港股IPO,市场曾传募资规模约3亿美元,但云顶新耀并未在招股书中披露募资金额。据悉,募资资金将用于进行临床试验、扩展药品管线、商业化候选药物等活动。
云顶新耀已经与全球的生物制药公司建立强大的关系,有系统地在各重点治疗领域中筛选及评估具有差异化、处于后期、已规避风险的资产。
你看好云顶新耀的发展吗?你认为云顶新耀能成功在港股上市吗?欢迎评论区留言讨论。




















评论