樊春海院士课题组2019年研究成果汇总

樊春海,上海交通大学化学化工学院王宽诚讲席教授,中国科学院院士。主要研究方向为生物传感与成像、DNA纳米技术与DNA计算和生物光子学。
课题组主要研究领域:
1. 生物传感与成像
2. DNA纳米技术与DNA计算
3. 生物光子学
以下对樊春海院士研究团队2019年的部分研究工作进行归纳,供大家学习交流。
(以通讯作者和0nline时间为主,如有疏漏,欢迎指正)
一、DNA折纸术
Nature Commun.:用DNA折纸成核剂指导curli聚合
原纤维的生理或病理学形成通常依赖于精确控制动力学和结构特征的分子级成核剂。然而,对蛋白质成核剂如何介导细胞中原纤维形成的机制的理解仍然难以捉摸。于此,上海科技大学钟超副教授和上海交通大学樊春海教授等人开发了一种修饰CsgB的DNA折纸(CB-折纸),以模拟大肠杆菌生物膜中诱导curli聚合的蛋白质成核剂。
实验表明,CB折纸指导curli亚基CsgA单体形成寡聚物,然后通过增加主要途径的增殖速率来加速原纤维形成。原纤维可以分别以远离(离开模式)或走向成核剂(到达模式)的方式加速生长,意味着CsgB的两个不同作用:作为成核位点和作为捕获位点以捕获附近生长的纳米原纤维。curli聚合遵循典型的stop-and-go动力学,但与独立的原纤维生长相比,表现出更高的瞬时伸长率。因此,该折纸成核剂提供了一个体外平台,用于机械探测分子成核并控制用于仿生纳米技术的定向原纤维聚合。
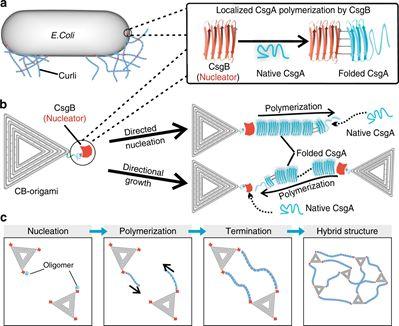
Mao, X., Li, K., Liu, M. et al. Directing curli polymerization with DNA origami nucleators. Nat Commun 10, 1395 (2019)
https://doi.org/10.1038/s41467-019-09369-6
2. Nature Commun.:非经典DNA金属化反应编程DNA折纸图案
DNA序列杂交的固有特异性已被广泛开发用于生物工程应用。但是,DNA的结构潜力尚未被开发用于创建基于非经典DNA的反应。于此,上海交通大学樊春海教授和同济大学柳华杰教授等人开发了一种DNA折纸启用的高度局部化金属化反应,用于具有10 nm分辨率的固有金属化图案。
理论和实验研究均表明,低价金属离子(Cu2+和Ag+)与二维DNA折纸上规定的突出簇状DNA(pcDNA)中的DNA碱基强烈配位,从而导致柔性pcDNA链对位点特异性的pcDNA缩合的有效吸引。研究人员发现金属化反应选择性地发生在规定的位置,而不发生在折纸基板上。此策略通常适用于在全DNA基板上以接近统一的效率对字母、数字和几何形状进行自由样式的金属绘画。研究人员进一步制造了单层和双层纳米级印刷电路板(nano-PCB)模仿物,为纳米电子和纳米光子应用的生物启发性制造提供了启发。

Jia, S., Wang, J., Xie, M. et al. Programming DNA origami patterning with non-canonical DNA-based metallization reactions. Nat Commun 10, 5597 (2019)
https://doi.org/10.1038/s41467-019-13507-5
3. JACS: 使用DNA在特定位点组织末端特定点的SWCNT
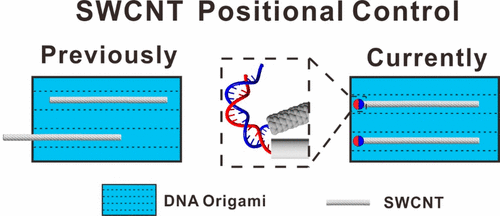
Hao Pei, Ruojie Sha, Xiwei Wang, Ming Zheng, Chunhai Fan, James W. Canary, and Nadrian C. Seeman. Organizing End-Site-Specific SWCNTs in Specific Loci Using DNA. Journal of the American Chemical Society 2019 141 (30), 11923-11928
https://doi.org/10.1021/jacs.9b03432
4. Nature Commun. DNA折纸加密技术用于安全通信
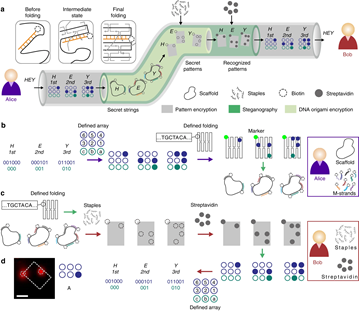
Zhang, Y., Wang, F., Chao, J. et al. DNA origami cryptography for secure communication. Nat Commun 10, 5469 (2019)
https://doi.org/10.1038/s41467-019-13517-3
二、DNA编程组装
5. Nature Materials: 用单链DNA精准编程纳米粒子
自然界已经进化出在单个生物聚合物中编码信息的策略,以编程具有特征性化学计量、正交性和可重构性的生物分子相互作用。然而,用于编程分子反应或组装的合成方法通常依赖于使用多条聚合物链(例如,斑片状颗粒)。于此,上海交通大学樊春海院士和荷兰格罗宁根大学诺奖得主Ben L. Feringa等人展示了一种利用含有聚腺嘌呤(polyA)的单链DNA编码器来图案化具有价键类似物的胶体金纳米粒子的方法。
通过用交替的polyA/非polyA结构域编程每个编码器的顺序、长度和序列,研究人员合成了具有n价的可编程类原子纳米粒子(PANs),可用于组装一系列具有不同组成、大小、手性和线性的低配位胶体分子。此外,利用PANs的可重构性,研究人员展示了动态胶体键断裂和键形成反应、结构重排甚至布尔逻辑运算的实现。这种方法可能有助于生成响应性功能材料,以用于不同的技术领域。
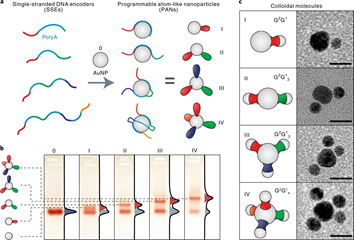
Yao, G., Li, J., Li, Q. et al. Programming nanoparticle valence bonds with single-stranded DNA encoders. Nat. Mater. (2019)
https://doi.org/10.1038/s41563-019-0549-3
6. Nature Commun.: 编程DNA发夹片共聚用于体外程序性超分子组织
通过蛋白质或蛋白质/核酸复合物的细胞内超分子聚合形成生物细丝是在可编程和时空控制下维持细胞和基因组完整性的。于此,中科院上海应用物理研究所樊春海院士与厦门大学田中群院士等人设计了一种受生物启发的,类似于催组装(catassembly)的等温链增长方法,将DNA发夹片(DHTs)聚合成具有按需组成、链长和功能的纳米纤维。
通过设计具有特定形状的分子内氢键的亚稳态DNA发夹,制备了两种类型的DHT单体用于共聚,具有高协同性和低分散指数。定量的单分子切割方法表明,含有托脚的DHT基序的催化开口会引发了连续的分支迁移,并自主地传播形成具有交替片单元的共聚物。研究人员发现这些形状确定的超分子纳米结构以一种刚性依赖的方式成为活体哺乳动物细胞有效内吞的基质。因此,这种类似于催组装的体外重建方法为理解生理和病理条件下生物丝的结构-功能关系提供了线索。
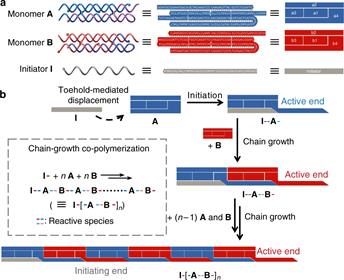
Zhang, H., Wang, Y., Zhang, H. et al. Programming chain-growth copolymerization of DNA hairpin tiles for in-vitro hierarchical supramolecular organization. Nat Commun 10, 1006 (2019)
https://doi.org/10.1038/s41467-019-09004-4
三、药物载体
7. Angew:对近红外光响应的H2S活化纳米诊疗平台
开发对近红外光响应的纳米平台为实现精确的癌症药物随需释放提供了新的方法。华东理工大学赵春常教授、中科院上海应用物理研究所诸颖博士和上海交通大学樊春海教授合作,利用H2S介导的反应原位生成了一种近红外光热试剂并将其用于成像和光控药物释放,该试剂具有靶向治疗具有丰富H2S的癌症的能力。
实验结果表明,该纳米平台可被H2S激活并产生NIR II发射,也能被红外光控制以释放药物喜树碱-11。实验在HCT116荷瘤小鼠模型上证明该纳米平台可显著抑制肿瘤生长,副作用也很低。因此,这一研究所开发的纳米诊疗平台也为实现NIR II成像指导的精确医学提供了新的思路。

BenShi, Ning Ren, Ying Zhu, Chunhai Fan, Chunchang Zhao. et al. A TheranosticNanoplatform with Hydrogen Sulfide-Activatable NIR Responsiveness forImaging-Guided On-Demand Drug Release. Angewandte Chemie International Edition.2019
https://onlinelibrary.wiley.com/doi/10.1002/anie.201909883
8. Nature Commun.:核酸框架体作为程序化载体用于经皮肤给药
具有纳米结构的DNA有着良好的生物相容性、均匀性和通用性,是一种很有前途的药物载体。然而,在全身给药后,血清会使其快速解体导致它在靶点部位的生物利用度较低,这也严重阻碍了其在生物医学领域的应用。新加坡南洋理工大学Chenjie Xu和上海交通大学樊春海教授等人设计不同形状和大小的核酸框架体(FNAs),并且研究了它们对小鼠和人类皮肤外植体的穿透性。
皮肤组织学实验表明,这种渗透的程度与尺寸大小相关,尺寸小于75 nm的FNAs 可以有效地渗透到真皮层,17 nm的四面体FNAs具有出最大的穿透距离(350微米)。并且在穿透皮肤时,FNAs的结构仍然保持完整性。实验采用小鼠黑色素瘤作为模型,相对于负载在脂质体和聚合物纳米颗粒中的阿霉素或游离的阿霉素来说,负载在FNAs上的阿霉素的药物积累和肿瘤抑制效果具有2倍的提高。
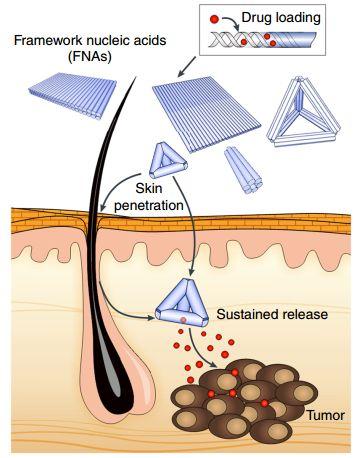
Wiraja, C., Fan, C.H., Xu, C.J. et al. Framework nucleic acids asprogrammable carrier for transdermal drug delivery. Nature Communications, 2019.
https://doi.org/10.1038/s41467-019-09029-9
9. ACS AMI: 磁性DNA纳米爪模仿病毒捕获细胞
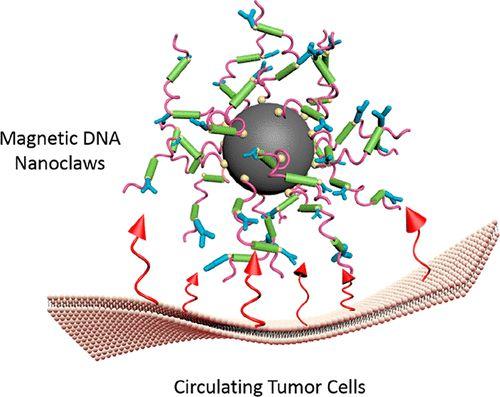
Zhiru Wang, Weiwei Qin, Jialang Zhuang, Minhao Wu, Qian Li, Chunhai Fan, and Yuanqing Zhang. Virus-Mimicking Cell Capture Using Heterovalency Magnetic DNA Nanoclaws. ACS Applied Materials & Interfaces 2019 11 (13), 12244-12252
https://doi.org/10.1021/acsami.8b21998
四、等离基元纳米光学
10. Chem. Rev.:多组分等离基元纳米颗粒---从异质结构纳米颗粒到胶体复合纳米结构
等离基元纳米结构具有独特的、多用途的光电特性,近十年来得到了广泛的研究。然而,等离基元纳米结构的全部潜力尚未得到充分开发,特别是具有单调性质的单组分均质结构,添加用于制备多组分纳米颗粒的新组分可能会导致新的或未预期的性能。于此,首尔大学Jwa-Min Nam和上海交通大学樊春海教授等人将术语“多组分纳米颗粒”定义为由两个或多个具有独特材料组成、形状或大小的凝聚纳米级域组成的混合结构。
回顾并讨论了有效组合多组分以形成具有新的或改进的等离基元功能的杂化纳米粒子的设计原理和合成策略。特别是,精确地合成多种多样的多组分等离基元纳米结构,限制了等离基元异质结构全部潜能的实现。为了应对这一挑战,已经报道了几种合成方法来形成各种不同的多组分等离基元纳米颗粒,主要基于非均相成核、原子替换、载体吸附和生物分子介导的组装。
此外,还报道了多组分等离激元纳米粒子的独特和协同功能,如原始材料特性的结合、精细调谐的等离基元共振和耦合、增强的光-物质相互作用、几何诱导极化以及等离基元诱导的能量和电荷在异质界面上的转移。这些等离激元纳米粒子包括异质结构纳米粒子和复合纳米结构,是通过直接合成以及物理力或生物分子介导的组装而制备的,它们在等离基元介导的能量转移、磁等离子体、超分子和纳米生物技术等方面具有巨大的潜力。

Minji Ha, Jae-Ho Kim, Myunghwa You, Qian Li, Chunhai Fan, and Jwa-Min Nam. Multicomponent Plasmonic Nanoparticles: From Heterostructured Nanoparticles to Colloidal Composite Nanostructures. Chemical Reviews 2019 119 (24), 12208-12278
https://doi.org/10.1021/acs.chemrev.9b00234
11. JACS: 等离基元纳米标记用于单细胞中的超级多重成像

Jianlei Shen, Le Liang, Mingshu Xiao, Xiaodong Xie, Fei Wang, Qian Li, Zhilei Ge, Jiang Li, Jiye Shi, Lihua Wang, Li Li, Hao Pei, and Chunhai Fan. Fractal Nanoplasmonic Labels for Supermultiplex Imaging in Single Cells. Journal of the American Chemical Society 2019 141 (30), 11938-11946
https://doi.org/10.1021/jacs.9b03498
12. ACS Nano: 具有活性等离基元迁移的手性大分子

Tiantian Man, Wei Ji, Xiaoguo Liu, Chuan Zhang, Li Li, Hao Pei, and Chunhai Fan. Chiral Metamolecules with Active Plasmonic Transition. ACS Nano 2019 13 (4), 4826-4833
https://doi.org/10.1021/acsnano.9b01942
除此之外,樊春海院士课题组还有一些生物传感方向的研究以及与其他研究人员合作的相关研究,感兴趣的可以参考课题组网站或者Pubmed上进行学习。
课题组网站:http://physbio.sinap.ac.cn/zucheng/fch.htm
Pubmed:https://www.ncbi.nlm.nih.gov/pubmed?cmd=search&term=Chunhai%20Fan
樊春海院士简介

樊春海,教授,博士生导师。1996年与2000年期间在南京大学分别获得本科和博士学位,后在圣芭芭拉加州大学从事博士后研究(导师:2000年诺贝尔化学奖得主Alan J. Heeger教授)。美国化学会ACS Applied Materials & Interfaces副主编,Advanced Healthcare Materials, ACS Sensors, ChemBioChem等杂志编委。
至今累计在Nature、Nature子刊、Science子刊等发表SCI论文400余篇。
2004年以来,樊春海教授先后入选中国科学院百人计划,国家杰出青年基金资助。2012-2016年任科技部纳米973首席科学家。入选美国科学促进会(AAAS)、国际电化学学会(ISE)和英国皇家化学会(RSC)会士,2019年当选中国科学院院士。连续六年入选“全球高被引科学家”。获2019年度何梁何利基金科学与技术创新奖、美国化学会“测量科学进展讲座奖”和第十二届“谈家桢生命科学创新奖”。
纳米生物医学最前沿
NanoLabs 微信公众号
你值得拥有





















评论