南工大冯超课题组:实现了芳基偕二氟环丙烷的1,3-氟烯丙基化

导语
三氟甲基广泛存在于药物分子中,如抗抑郁药物盐酸氟西汀(Prozac), 抵抗艾滋病毒的特效药物(Efavirenz)以及治疗肿瘤的口服药物(Sorafenib)等。因此,将三氟甲基引入到有机骨架中的方法一直是合成化学领域的热门研究方向。已报道的合成策略主要可以分为以下两类:1、利用三氟甲基试剂进行直接的三氟甲基化;2、对含三氟甲基的合成砌块进行官能化。但是,商品化的三氟甲基试剂通常价格昂贵,并且原子利用率低;而廉价易得的含三氟甲基合成砌块较为有限。因此,开发新型的构筑含三氟甲基复杂结构的方法依然具有很大的价值。近日,南京工业大学冯超教授课题组利用可见光促进的单电子氧化策略,活化芳基偕二氟环丙烷接受氟负离子的亲核进攻,通过F2C−F键的形成巧妙地构筑了三氟甲基,实现了芳基偕二氟环丙烷的1,3-氟烯丙基化(Org. Lett.2020, DOI:10.1021/acs.orglett.0c03268)。
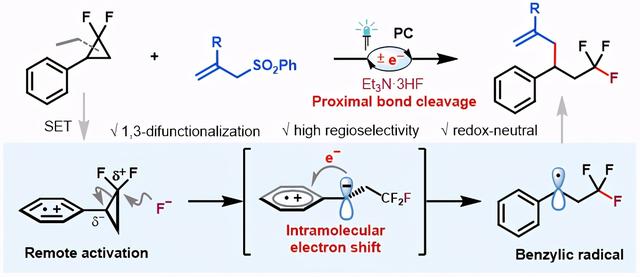
图1. 可见光促进的偕二氟环丙烷1,3-氟烯丙基化(来源:Org. Lett.)
冯超教授课题组简介
冯超教授课题组的研究方向主要为含氟化合物合成新方法及可见光氧化还原催化不饱和体系双官能化。
冯超教授简介

冯超,南京工业大学教授、博士生导师。2008-2012年就读于新加坡南洋理工大学,获博士学位,师从罗德平教授;2012-2016年在罗德平教授课题组开展博士后研究工作,致力于碳氢键官能化反应的研究;2016年全职加入南京工业大学先进化学制造研究院开展独立研究工作,以发展具有潜在药用价值和生物活性骨架的构建方法为导向开展系统的科学研究,主要研究方向为氟化学以及可见光氧化还原催化领域,研究成果发表于J. Am. Chem. Soc., Angew. Chem. Int. Ed., Nat. Commun. 等国际高水平期刊上,2018年荣获Thieme Chemistry Journal Award。
前沿科研成果
可见光促进偕二氟环丙烷的选择性1,3-氟烯丙基化
由于氟原子的强诱导效应以及氟与烯烃的p-π共轭效应,偕二氟烯烃的偕二氟碳原子具有一定的电正性,另一个烯烃碳原子则带有一定的电负性。因此它更容易发生亲核加成而不是亲电加成。基于偕二氟烯烃的此种性质,冯超教授开发出一系列氟亲核加成诱导的偕二氟烯烃官能团化反应(图2. J. Am. Chem. Soc. 2016, 138, 15869-15872; Angew. Chem. Int. Ed. 2017, 56, 9872-9876)。α-三氟甲基碳负离子通常情况下不稳定,容易被质子化或者发生氟消除。因此富电子的偕二氟烯烃在氟亲核加成诱导的烯丙基化反应中兼容性非常不理想。针对该问题,冯超教授给出的解决方案是,通过可见光促进的单电子氧化过程对富电子偕二氟烯烃进行活化,有效促进氟亲核加成,并将不稳定的α-三氟甲基碳负离子中间体转化为相对较稳定的α-三氟甲基自由基,实现了其氟烯丙基化(Angew. Chem. Int. Ed. 2019, 58, 3918-3922)。最近,在这些工作的基础上,冯超教授课题组通过可见光促进的单电子氧化过程,对富电子的偕二氟环丙烷进行活化,利用偕二氟原子稳定α-碳正离子的性质,精准控制氟负离子对环丙烷亲核进攻的位点选择性,构筑三氟甲基,实现偕二氟环丙烷结构的开环1,3-氟烯丙基化。
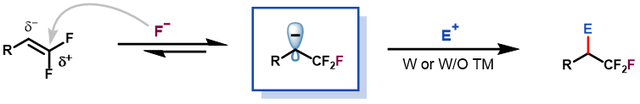
图2. 偕二氟烯烃氟负亲核加成诱导的官能团化反应(来源:Org. Lett.)
作者首先利用激发态下单电子氧化能力较强的[Ir(dF(CF3)ppy)2(5,5′-d(CF3)bpy)](PF6) (PC-II, ERed = +1.69 V vs. SCE in MeCN) 作为光催化剂,对甲氧基苯基偕二氟环丙烷作为反应模板底物,经过一系列的反应条件筛选成功以74%的分离收率得到目标产物。通过对底物的普适性进行调查,作者发现各种具有烷氧基取代基的富电子底物均能以较好的收率获得目标产物。对位苯基(3d)或者烷基(3e)取代的芳基二氟环丙烷需要以氧化电势更高的吖啶类型光催化剂才能得到目标产物。邻位甲氧基取代的底物(3m-3o, 3t)由于位阻的原因反应效果较差仅能以中等及以下收率得到目标产物。当三元环结构2号位芳基取代(3w)或者偕二烷基取代(3v)时,氟进攻位点将选择性地转为芳基碳或者偕二甲基碳上,推测的原因是芳基或者偕二甲基具有很好的稳定正电荷的能力。反应以廉价易得的三乙胺三氢氟酸盐作为亲核试剂。对烯丙基砜的底物范围进行考察,作者发现适用的底物主要包括烯烃上有拉电子基团的烯丙基砜。可能的原因是氟进攻开环后生成的苄基自由基较为富电子,趋向于与缺电子的烯烃发生自由加成反应。为了进一步考察反应的实用性,作者设计合成了具有表雄酮与薄荷醇结构的烯丙基砜,发现反应也能以中等及以上收率生成目标产物。
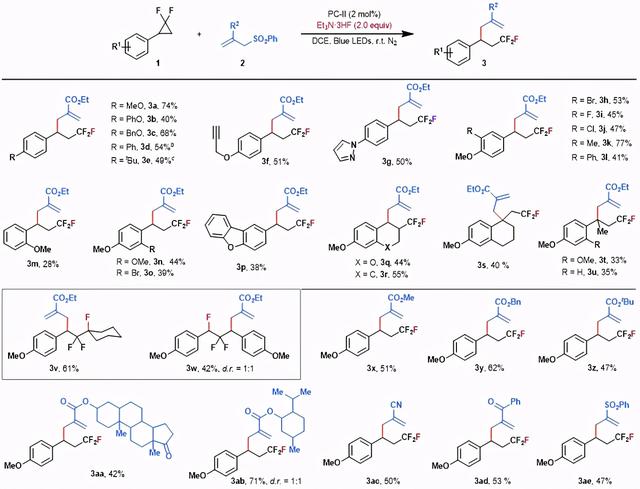
图 3. 可见光促进偕二氟环丙烷1,3-氟烯丙基化反应的底物范围(来源:Org. Lett.)
为了进一步验证反应的机理,作者进行了一系列控制实验。荧光淬灭实验表明反应中仅有芳基偕二氟环丙烷能够淬灭光催化剂。普通的非活化偕二甲基取代环丙烷4a在反应中也具有较好的反应效果。当2位与3位均不存在取代基的芳基环丙烷4b投入反应中时,并不能得到目标产物,且反应原料大量剩余。标准条件下加入1.0当量的自由基捕捉试剂TEMPO或BHT时,反应被完全抑制。在自由基钟实验中,作者成功以39%的分离得到了1,6氟烯丙基化产物6a(E/Z = 1:6.7)。实验结果进一步印证了反应生成了苄基自由基。同种类型的苄基自由基已有大量文献报道,通过三氟甲基自由基对烯烃并在空气或者氧气的条件下可转化为芳基三氟乙基酮。当反应在不加烯丙基砜,且氧气的氛围下,作者确实能得到73%的芳基三氟乙基酮产物7a。进一步对其它的卤素负离子进行考察,作者发现2,6-二甲基吡啶盐酸盐为亲核试剂的条件下,其亲核进攻的位点失去了选择性。这些结果都证实了作者推测的单电子氧化活化芳基二氟环丙烷-氟离子亲核进攻-三元环开环烯丙基化历程为合理的反应机理。
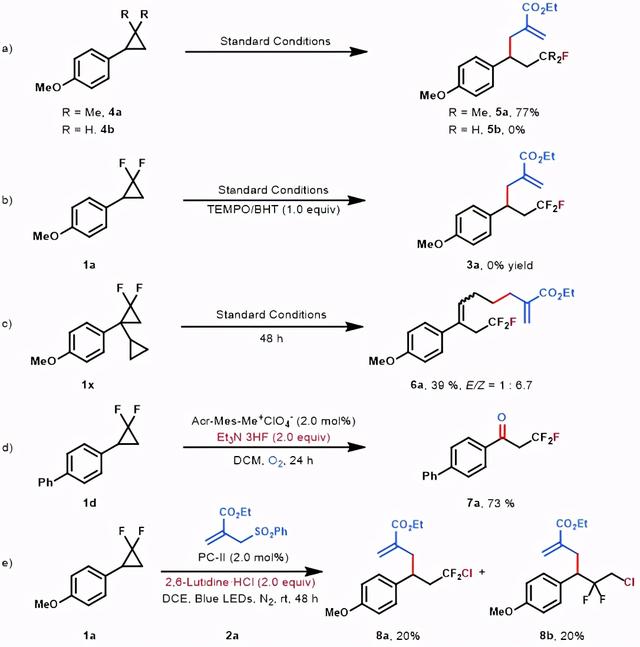
图 4. 控制实验(来源:Org. Lett.)
该工作近期以“Visible-Light-Promoted Regioselective 1,3-Fluoroallylation of gem-Difluorocyclopropanes”为题发表于Org. Lett.(DOI: 10.1021/acs.orglett.0c03268)上。该论文第一作者为南京工业大学博士研究生刘海东。通讯作者为南京工业大学冯超教授。研究工作得到了国家自然科学基金(21871138)以及江苏省自然科学基金(BK20170984),江苏省特聘教授计划以及双创人才计划的资助。





















评论