如何看待疫苗保护力随时间推移而下降的问题
疫苗接种后,对我们的保护力会随着时间推移而下降。
这其实是一个很普遍的现象。比较出名的有流感疫苗。它就需要每年注射一次。
新冠疫苗也存在这个问题。
在上市前,辉瑞-BNT疫苗的3期临床试验,即严格随机对照研究证实:在第2剂注射的7天后开始追踪,中位追踪时限2个月,最终的疫苗保护率是95%有效[1-2]。
但请注意,观察时限是2个月。
如果延长时间呢?
近期,梅奥诊所在Medrxiv上传了一份研究报告[3]。如在2020年12月接种疫苗,而看2021年1月到7月的保护率变化:Moderna 疫苗在预防感染的保护率从 93.3% 降至 76%,而辉瑞疫苗更是从 86.1% 下降至 42%。
但请注意,梅奥诊所做的是一个真实世界的“配对研究”;其配对的依据是:年龄、性别、接种时间[3]。
为什么要根据接种时间做配对呢?因为,如不做时间上的配对,疫苗的保护率计算会出现错误。
已知如下数据:
截止9月4日,往前推的28天内:新加坡共新增2671起本土病例,其中1953人已完成全程疫苗接种,452人未接种。

来自微博的“新加坡眼”的图片

来自微博的“新加坡眼”的图片
截至9月3日,新加坡约83%人口(876万5482人)接种至少一剂疫苗,约81%人口已完成疫苗全程接种(数据来自新加坡眼)。
而新加坡的完全接种疫苗数是7100040
完全没接种疫苗的人口数则是1490132
那么计算疫苗的保护率是:
(未接种人群的感染率-已完全接种人群的感染率)÷未接种人群的感染率=疫苗保护率
(452÷1490132-1953÷7100040)÷(452÷1490132)=9.3166%
但这个9.3166%是不可靠的。因为并没有根据接种时间做匹配。而且也没有根据年龄做分组分析。毕竟不同年龄段的感染风险是不同的。
根据“接种时间+同年龄段”匹配,计算出来的数据就很可能大大不同。
1,不根据接种时间做匹配,那么就会有一些曾经感染者被我们忽视!
请注意,我们根据的数据是「截止9月4日,往前推的28天内,新加坡共新增2671起本土病例」。但我们并不清楚1490132未接种人群里有多少人曾经感染过新冠。一旦感染过新冠,他们就可能获得持续的抵抗力。这种抵抗力未必弱于接种疫苗。
已知新加坡到今天约6万多人感染过新冠。其中相当部分在感染时尚未接种过疫苗。
2,不根据年龄做匹配,就会把感染低风险人群纳入计算
未接种疫苗的人群里相当部分是12岁以下;因为新加坡目前的政策是对12岁以上人群接种疫苗。
研究发现:相对成年人,12岁以下感染新冠的风险显著偏低[4-5];他们即便感染,其相当部分是无症状感染。
比如 ,加拿大一个包含2463例在社区环境中(即不在急诊室)接受SARS-CoV-2检测的儿童感染人群,其中714 人(35.9%)是无症状感染[6]。
为了避免辛普森悖论(具体讨论参考“庄时利和”先生的文章),我们要根据不同年龄段做分组匹配。然后再行对照研究。
但上述计算时,我们没有做年龄分组匹配讨论,也没有排除掉那些曾经感染过新冠的人群。所以9.3166%是不可靠的。
梅奥诊所在Medrxiv上传了那份研究报告[3]是有根据年龄、接种时间做匹配的。根据上述因素做匹配然后追踪6个月的数据是:Moderna 疫苗在预防感染的保护率从 93.3% 降至 76%,而辉瑞疫苗更是从 86.1% 下降至 42%。
这说明是否合理匹配,对数据统计的结论有较大影响。
不看感染率,我们看重症率如何?
在所有完成接种但仍染疫的病患当中,0.1%为ICU重症,1.0%为输氧重症,98.9%为无症状或轻微症状。
1953 (完成疫苗接种后的感染数)×0.1%=2
在未接种的病患当中,0.9%病逝,0.4%为ICU重症,5.8%为输氧重症,92.9%为无症状或轻微症状。
452 (未接种疫苗后的感染人数)×0.4%=2
疫苗对入ICU的保护率如下
(未接种人群的ICU率-已完全接种人群的ICU率)÷未接种人群的ICU率=疫苗保护率
(2÷1490132-2÷7100040)÷(2÷1490132)=79.01%
还是那句话,没有对年龄,对接种时间上的亚组分析,还是要小心辛普森悖论。另外,数据量较小,统计学误差风险较大。但初步可以看出,疫苗对预防重症的效果没有明显下降。
实际上,笔者撰写的同一个时间点,新加坡眼发布了一个新数据:截止9月5日,往前推28天内,新加坡有2784起本土病例,其中74%已完成全程疫苗接种,9%部分接种,17%未接种。
这里的ICU重症人群里没有疫苗完全接种者。可见这样的实时数据做分析是不那么靠谱的----统计误差太大。
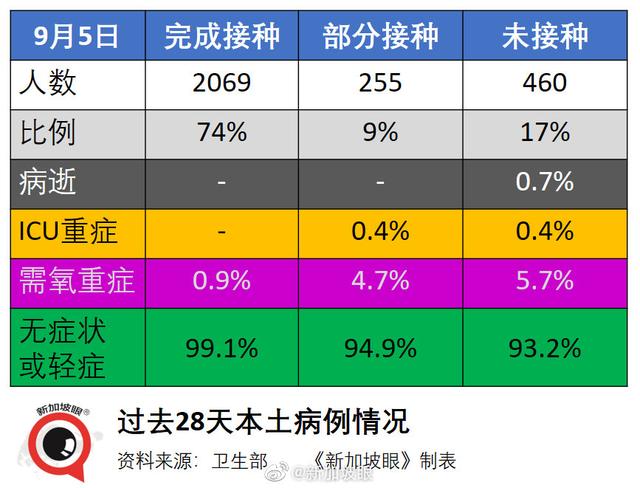
来自微博“新加坡眼”的图
参考资料:
1,FDA Briefing Document. Pfizer-BioNTech COVID-19 Vaccine. Vaccines and Related Biological Products Advisory Committee Meeting. December 10, 2020 https://www.fda.gov/media/144245/download (Accessed on December 09, 2020).
2,Polack FP, Thomas SJ, Kitchin N, et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N Engl J Med 2020; 383:2603.
3,Arjun Puranik, Patrick J. Lenehan, et al.Comparison of two highly-effective mRNA vaccines for COVID-19 during periods of Alpha and Delta variant prevalence. medRxiv preprint doi: https://doi.org/10.1101/2021.08.06.21261707;
4,Leidman E, Duca LM, Omura JD, et al. COVID-19 Trends Among Persons Aged 0-24 Years - United States, March 1-December 12, 2020. MMWR Morb Mortal Wkly Rep 2021; 70:88.
5,Götzinger F, Santiago-García B, Noguera-Julián A, et al. COVID-19 in children and adolescents in Europe: a multinational, multicentre cohort study. Lancet Child Adolesc Health 2020; 4:653.
6,King JA, Whitten TA, Bakal JA, McAlister FA. Symptoms associated with a positive result for a swab for SARS-CoV-2 infection among children in Alberta. CMAJ 2021; 193:E1.




















评论